��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��һ�������£����淴Ӧ��mA+nB pC�ﵽƽ�⣬����
pC�ﵽƽ�⣬����
(1) A��B��C�������壬����ѹǿ��ƽ��������Ӧ�����ƶ�����m+n��p�Ĵ�С��ϵ��?��
(2) A��C�����壬������B������ƽ�ⲻ�ƶ�����BӦΪ?̬��
(3) A��C�����壬����m+n = p������ѹǿ��ʹƽ�ⷢ���ƶ�����ƽ���ƶ��ķ������?��
(4) ���Ⱥ�ʹC���������ӣ�������Ӧ��?��Ӧ(ѡ����ȡ������ȡ�)��
�ο��𰸣���8�֣���1�� m+n��p?��2����̬��(��)Һ̬ ��3�������ƶ� ��4������
���������(1) ���淴Ӧ��mA+nB pC�ﵽƽ�⣬��A��B��C�������壬����ѹǿ��ƽ��������Ӧ�����ƶ�����˵������Ӧ���������Ŀ��淴Ӧ������m+n��p��
pC�ﵽƽ�⣬��A��B��C�������壬����ѹǿ��ƽ��������Ӧ�����ƶ�����˵������Ӧ���������Ŀ��淴Ӧ������m+n��p��
(2) ���淴Ӧ��mA+nB pC�ﵽƽ�⣬��A��C�����壬������B������ƽ�ⲻ�ƶ�����˵��BӦΪ��̬��(��)Һ̬��
pC�ﵽƽ�⣬��A��C�����壬������B������ƽ�ⲻ�ƶ�����˵��BӦΪ��̬��(��)Һ̬��
(3) ���淴Ӧ��mA+nB pC�ﵽƽ�⣬�� A��C�����壬����m+n��p������ѹǿ��ʹƽ�ⷢ���ƶ�����˵��A��B��������һ���ǹ����Һ�壬��ѹƽ�����淴Ӧ�����ƶ�����ƽ���ƶ��ķ�����������ƶ���
pC�ﵽƽ�⣬�� A��C�����壬����m+n��p������ѹǿ��ʹƽ�ⷢ���ƶ�����˵��A��B��������һ���ǹ����Һ�壬��ѹƽ�����淴Ӧ�����ƶ�����ƽ���ƶ��ķ�����������ƶ���
(4) ���Ⱥ�ʹC���������ӣ���˵�������¶�ƽ��������Ӧ�����ƶ����������Ӧ�����ȷ�Ӧ��
�����Ѷȣ�һ��
2�������� ��9�֣���һ���ݻ�Ϊ500mL���ܱ������У�����5mol H2��2 mol CO����һ���¶Ⱥ�һ��ѹǿ�£��������·�Ӧ�ڣ�2H2(g) +CO(g) CH3OH(g)������5min��ﵽƽ��״̬������ʱ���������ѹǿ����ʼʱ��4/7����1����H2��Ũ�ȱ仯��ʾ�ĸ÷�Ӧ�����ʣ�2����ƽ��ʱCO��ת���ʣ�3�����¶��µ�ƽ�ⳣ��K
CH3OH(g)������5min��ﵽƽ��״̬������ʱ���������ѹǿ����ʼʱ��4/7����1����H2��Ũ�ȱ仯��ʾ�ĸ÷�Ӧ�����ʣ�2����ƽ��ʱCO��ת���ʣ�3�����¶��µ�ƽ�ⳣ��K
�ο��𰸣���1��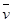 (H2) =1.2mol/��L��min��?
(H2) =1.2mol/��L��min��?
��2������CO��=C��Ӧ��CO��/ C��ʼ��CO����100%=75%
��3��K= C��CH3OH ��/ C��CO����C2��H2��="0.1875" ��mol/��L��-2
���������2H2(g) +CO(g) CH3OH(g)
CH3OH(g)
n0? 5? 2? 0
��n? 2x? x? x
n(ƽ��)? 5-2x? 2-x? x
����PV=nRT,�ں��¡������£���n0/ n(ƽ��)=P0/P(ƽ��)��
��5+2��/[(5-2x)+(2-x)+x]= P0/[4/7 P0]���ã�x=1.5 mol
(1)�ԣ�H2��=��2x/0.5L��/5min=1.2 mol/��L��min��
(2)CO��ת����=x/2=75%
K=3/(42��1)=0.1875��mol/��L��-2
�����Ѷȣ�һ��
3��ѡ���� ��һ���ܱ������У��õ����ʵ�����A��B�������·�Ӧ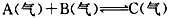 ��Ӧ�ﵽƽ��ʱ�������������A��B�����ʵ���֮����C�����ʵ�����ȣ���ʱA��ת����Ϊ
��Ӧ�ﵽƽ��ʱ�������������A��B�����ʵ���֮����C�����ʵ�����ȣ���ʱA��ת����Ϊ
[? ]
A��40%
B��50%
C��60%
D��70%
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� ��һ�������£���3molA ��1mol B �����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A��g��+B��g�� ?xC��g��+ 2D��g����2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8mol D �������C��Ũ��Ϊ0.2mol��L��1������գ�
?xC��g��+ 2D��g����2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8mol D �������C��Ũ��Ϊ0.2mol��L��1������գ�
��1��x=__________
��2������Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�����Ӧ����?���淴Ӧ����?���������ߡ����ͻ䣩
��3��B��ת����Ϊ_________��
��4�����жϸ÷�Ӧ�ﵽƽ��״̬��������________������ĸ��
A�����������ܶȲ���
B�������е�ѹǿ���ٱ仯
C������D�ķ�Ӧ����������B�ķ�Ӧ���ʵ�2��
D����λʱ��������3molA��ͬʱ����1molB
�ο��𰸣�x=1 �����ߣ����ߣ�40%��BC
���������������淴Ӧ���йؼ��㡢��������Է�Ӧ���ʵ�Ӱ�켰ƽ��״̬���жϡ�
��1��ƽ��ʱC��Ũ����0.2mol/L�������ʵ�����0.2mol/L��2��0.4mol����C��D�����ʵ���֮����1�U2������x��1.
��2�������¶����淴Ӧ���ʾ�������ģ��뷴Ӧ�Ƿ��Ȼ������ء�
��3�����ݷ�Ӧʽ��֪ÿ����0.2mol��C��������0.2mol��B������B��ת������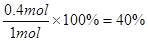 ��
��
��4����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ���������ʵ�Ũ�Ȼ��������ٷ����仯��״̬���ǻ�ѧƽ��״̬���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������У��������ݻ����Dz���ģ������ܶ�ʼ���Dz���ġ����ڷ�Ӧǰ����������DZ仯�ģ���ѹǿ�DZ仯�ģ���˵�ѹǿ���ٷ����仯ʱ�����ﵽƽ��״̬��C�з�Ӧ���ʷ����෴������������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ��D�з�Ӧ���ʷ�����ͬ������˵������ѡBC��
�����Ѷȣ�һ��
5������� ��14�֣���������Ҫ������Դ��������Ϊ�������õĹؼ��������ǵ�ǰ��ע���ȵ�֮һ��
��1�������������Դ����ȼ�ղ���Ϊ__________��
��2��NaBH4��һ����Ҫ�Ĵ������壬����ˮ��Ӧ�ﵽNaBO2���ҷ�Ӧǰ��B�Ļ��ϼ۲��䣬�÷�Ӧ�Ļ�ѧ����ʽΪ___________����Ӧ����1mol NaBH4ʱת�Ƶĵ�����ĿΪ__________��
��3������ɽ����л�������û�����ͱ�֮��Ŀ��淴Ӧ��ʵ������ͼ��⣺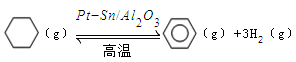 ��ij�¶��£�������ܱ������м��뻷���飬��ʼŨ��Ϊa mol/L��ƽ��ʱ����Ũ��Ϊbmol/L���÷�Ӧ��ƽ�ⳣ��K��_____��
��ij�¶��£�������ܱ������м��뻷���飬��ʼŨ��Ϊa mol/L��ƽ��ʱ����Ũ��Ϊbmol/L���÷�Ӧ��ƽ�ⳣ��K��_____��
��4��һ�������£���11ͼʾװ�ÿ�ʵ���л���ĵ绯ѧ���⣨���������л����
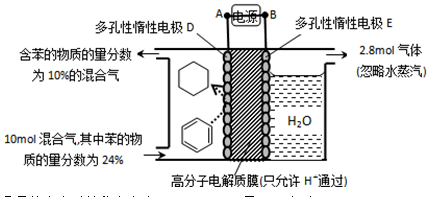
�ٵ����е����ƶ�����Ϊ____________��
������Ŀ�����ĵ缫��ӦʽΪ_________��
�۸ô���װ�õĵ���Ч��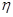 ��_____��
��_____��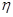 ��
�� ��100%������������С�����1λ��
��100%������������С�����1λ��
�ο��𰸣���1��ˮ��H2O?��2��NaBH4��2H2O=NaBO2��4H2����4NA��2.408��1024
��3��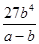 ?mol3/L3?��4����A��D ?��C6H6��6H����6e����C6H12?��64.3%
?mol3/L3?��4����A��D ?��C6H6��6H����6e����C6H12?��64.3%
�����������1��������ȼ�ղ�����ˮ��
��2����Ӧǰ��BԪ�صĻ��ϼ۲��䣬��Ӧǰ��BԪ�صĻ��ϼ۾��ǣ�3�ۣ���˷�ӦǰNaBH4����Ԫ�صĻ��ϼ��ǣ�1�ۡ�ˮ����Ԫ�صĻ��ϼ��ǣ�1�ۣ���˷�Ӧ�л����������ɣ���Ӧ�Ļ�ѧ����ʽΪNaBH4��2H2O=NaBO2��4H2����NaBH4����Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ����1molNaBH4�ڷ�Ӧ��ʧȥ4mol���ӣ�����Ŀ��4NA��2.408��1024��
��3��ƽ��ʱ����Ũ����b mol/L������ݷ�Ӧ�ķ���ʽ��֪���Ļ������Ũ����b mol/L������������Ũ����3 b mol/L����ƽ��ʱ�������Ũ��Ϊ��a��b��mol/L�����ڻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ������¶��·�Ӧ��ƽ�ⳣ��Ϊ ��
��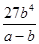 mol3/L3��
mol3/L3��
��4���ٱ����ɻ��������ڵ��ⷴӦ������ǻ�ԭ��Ӧ�����缫D���������缫E����������˵����е��ӵ�����������A��D��
�ڱ��õ��������ɻ�������Ŀ�������ڴ������ӽ���Ĥ�������������������ƶ�����缫��ӦʽΪC6H6��6H����6e����C6H12��
����������2.8mol���壬������Ӧ��������OH���ŵ����ɵ���������ת�Ƶ��ӵ����ʵ�����2.8mol��4��11.2mol�����������ı������ʵ�����xmol����ͬʱ���� xmol�����飬���ݵ缫��ӦʽC6H6��6H����6e����C6H12��֪�õ�������6xmol�����ݵ����غ��֪����������������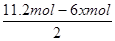 ��5.6mol��3xmol������
��5.6mol��3xmol������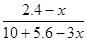 ?��0.1�����x��1.2����˴���װ�õĵ���Ч�ʣ�
?��0.1�����x��1.2����˴���װ�õĵ���Ч�ʣ� ��100%��64.3%��
��100%��64.3%��
�����Ѷȣ�һ��