微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下图是 10ml 量筒的一部分,数字XY之间相差 1ml,若 X=5,则量筒所盛液体的体积是
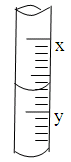
A.5.7 ml
B.4.4 ml
C.4.3 ml
D.6.3 ml
参考答案:C
本题解析:若 X=5,Y=4,每小格0.1mL,所以读数为4.3 ml,选C。
本题难度:简单
2、实验题 (6分)如图所示装置,在化学实验中十分常见,它可以作为制取气体、收集气体、性质验证、安全防护等多种作用,按要求回答相关问题:
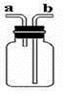
(1)干燥CO2气体时,广口瓶中可装入的试剂1是______________。
(2)除掉CO中混有的CO2,可以在广口瓶中盛装试剂2?溶液。
(3)用此装置可以用排气法收集CO2气体,应从导管口?进?出。(填a或b)
如果用此装置收集CO气体,应怎样操作,简述操作方法:
_________________________________________________________________________。
(4)广口瓶C中盛有BaCl2溶液,如果从b端通入CO2气体,甲同学说有沉淀生成,乙同学说没有沉淀出现。根据你所掌握的知识,判断其正确性,选择你同意的一方意见回答相关问题(两项全答计0分)。
I.我同意甲同学意见,得到的沉淀物质化学式为__________________。
II.我同意乙同学意见,如要出现沉淀,可以预先在广口瓶中加入一些试剂3,再通入CO2气体,立即会出现沉淀,则试剂3可以是_____________(填试剂名称或化学式)。
参考答案:(1)浓硫酸(1分)。?(2)NaOH(1分,其他合理答案均可给分)。
(3)b? a (1分)?将广口瓶盛满水(1分),从a端通入气体,水从b端排出(1分)。
(4)I.________________。
II. NaOH溶液(1分,其他合理答案均可给分)
本题解析:(1)CO2时酸性氧化物,应该用浓硫酸干燥。
(2)CO2作为一种酸性氧化物,能溶于碱中,所以可以选择试剂氢氧化钠溶液。
(3)CO2的密度大于空气的,所以应该是b进a出。
(4)由于碳酸钡不溶于水,但能溶于酸中,所以不会产生沉淀。所以要想得到沉淀,则必须使溶液呈碱性,因此加入氢氧化钠溶液即可。
本题难度:一般
3、选择题 下列各图所示的实验原理、方法、装置和操作正确的是(苯,一种密度比水小的不溶于水的有机溶剂) (?)?
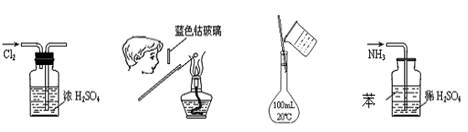
①? ②? ③? ④
A.①干燥Cl2
B.②检验K2CO3中的K+
C.③配制150 mL 0.10 mol・L-1盐酸
D.④吸收NH3
参考答案:B
本题解析:A项:干燥气体时导气管应该“长进短出”,故错;C项:配置150ml溶液不能用100ml的容量瓶,故错;D项:会造成倒吸,故错。故选B。
点评:本题考查较为综合,涉及药品的称量、气体的收集、溶液的配制以及防倒吸等实验基本操作,题目难度不大,注意化学实验的基本操作要点。
本题难度:一般
4、实验题 (15分)某校某班化学兴趣小组进行了下列两项试验活动:(1)探究草酸(H2C2O4)与高锰酸钾溶液在不同条件下反应的快慢;(2)测定草酸晶体的纯度。已知:①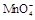 在酸性环境下的还原产物是
在酸性环境下的还原产物是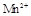 ;②草酸是二元弱酸。
;②草酸是二元弱酸。
Ⅰ.探究草酸与高锰酸钾溶液在不同条件下反应的快慢
取4支试管,分别加入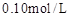 的草酸溶液
的草酸溶液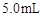 ,按下表中四种方案分别加入相应的试剂,使其发生反应。四支试管中均可观察到有气泡产生,且溶液的颜色变化都为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如下表所示(表中“―”表示未加入该试剂)。
,按下表中四种方案分别加入相应的试剂,使其发生反应。四支试管中均可观察到有气泡产生,且溶液的颜色变化都为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如下表所示(表中“―”表示未加入该试剂)。
实验
编号
| 反应温度
(利用水浴加热)
| 稀硫酸溶液
| 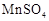 固体 固体
| 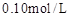
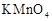 溶液 溶液
| 褪色时间
|
1
| 65℃
| ―
| ―
| 1.0mL
| 100s
|
2
| 65℃
| 10滴
| ―
| 1.0mL
| 90s
|
3
| 75℃
| 10滴
| ―
| 1.0mL
| 40s
|
4
| 75℃
| 10滴
| 加入少许
| 1.0mL
| 3s
|
根据以上4组实验,可以得出的结论主要有_______________________________。
Ⅱ.测定草酸晶体的纯度
用托盘天平称取草酸晶体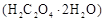 样品
样品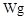 ;配制成
;配制成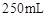 溶液;每次移取25.00mL该溶液于锥形瓶中,用0.1 0mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2―3次。请回答:
溶液;每次移取25.00mL该溶液于锥形瓶中,用0.1 0mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2―3次。请回答:
(1)实验中需要用到的玻璃仪器除了玻璃棒、烧杯、锥形瓶、胶头滴管、250mL容量瓶外还需要的一种玻璃仪器是____________。(填仪器名称)
(2)上述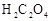 溶液与酸性
溶液与酸性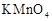 溶液反应的离子方程式为_________。
溶液反应的离子方程式为_________。
(3)若滴定过程中平均消耗酸性高锰酸钾溶液VmL,则草酸晶体的纯度为_______(以含W、V的表达式表示)。
参考答案:(13分)Ⅰ.①稀硫酸可使上述反应速率加快;②升高温度,反应速率加快;
③Mn2+作该反应的催化剂,可加快反应速率。(每个结论2分,其它合理答案均给分)(6分)
Ⅱ.(1)酸式滴定管(2分)
(2)5H2C2O4+2MnO4-+6H+=2Mn2++8H2O+10CO2↑(3分)
(3)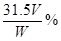 (其它合理表达式均给分)(4分)
(其它合理表达式均给分)(4分)
本题解析:Ⅰ.根据反应中改变的条件及褪色时间长短可知,可以得出的结论有.①稀硫酸可使上述反应速率加快;②升高温度,反应速率加快;③Mn2+作该反应的催化剂,可加快反应速率。
Ⅱ.(1)滴定实验中小于滴定管,而酸性高锰酸钾溶液需要放在酸式滴定管中。
(2)草酸的氧化产物是CO2,而高锰酸钾的还原产物是硫酸锰,所以根据电子的得失守恒及质量守恒定律可知,该反应的方程式是5H2C2O4+2MnO4-+6H+=2Mn2++8H2O+10CO2↑。
(3)稀释高锰酸钾的物质的量是0.0001Vmol,所以根据方程式可知,草酸的物质的量是0.00025Vmol,则原溶液中草酸的物质的量是0.00025Vmol×10=0.0025Vmol。因此草酸晶体的纯度为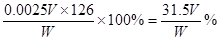 。
。
本题难度:一般
5、选择题 下图所示的操作,其中正确的是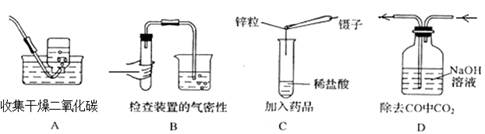
参考答案:B
本题解析:A项:排水法收集气体,气体中含有水份不干燥,故错;C项:镊子要垂直,故错;D项:除杂应长进短出,故错。故选B。
点评:本题考查的是化学实验的基本操作的相关知识,题目难度不大,平时多注意基础知识的学习。
本题难度:简单