?
参考答案:(16分)(1)(4分)Na2O2? 2
(2)①(2分)假设3:是Na2O2与Na2CO3的混合物 [说明:不可能有NaOH,因为在空气中即使吸水生成有NaOH,但时间长了也与CO2反应生成了Na2CO3]
②
实验步骤
预期现象和结论
?
假设2或假设3成立(2分,或假设1不成立)
步骤2:另取少量固体于试管中加适量蒸馏水(2分),再滴入酚酞溶液(2分)[或,用带火星的火柴伸入试管口] [如果向步骤一的溶液中直接滴酚酞,或用KI淀粉液,扣1分]
若滴入酚酞溶液后先变红后褪色(或溶液变蓝色,2分)[或带火星的火柴复燃],则假设1或假设3成立(1分);若红色不褪色,则假设2成立(1分)
本题解析:(1)反应中的电子转移为: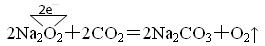 ,是Na2O2发生了自身氧化还原反应,既是氧化剂又是还原剂,每生成每生成1molO2则转移了2mol电子 ,是Na2O2发生了自身氧化还原反应,既是氧化剂又是还原剂,每生成每生成1molO2则转移了2mol电子
(2)①Na2O2在空气中主要是可以和CO2、H2O反应分别生成Na2CO3与NaOH,而因为NaOH在空气中与CO2反应最终也生成Na2CO3,所以不可能有NaOH,故有三种假设情况
②实际上就是CO32―及Na2O2的检验。
本题难度:一般
2、选择题 纯碱和小苏打是厨房中两种常见用品,它们都是白色固体,下列区分它们的说法正确的是(?)
A.先将两样品配成溶液,分别加入澄清石灰水,无白色沉淀生成的是小苏打
B.用洁净铁丝蘸取两种样品在煤气灯火焰上灼烧,火焰颜色为黄色的是小苏打
C.分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打
D.用两只小玻璃杯,分别加入少量的两种样品,再加入等浓度的食醋,产生气泡速率较快的是小苏打
参考答案:D
本题解析:A 错误,分别加入澄清石灰水,都会有白色沉淀生成
B 错误,因为都是钠盐,做焰色反应,都是黄色
C 错误,碳酸氢钠受热分解会得到碳酸钠、水、二氧化碳,所以会有残留物生成
D 正确,碳酸氢钠与酸反应产生的气泡快。
本题难度:一般
3、填空题 (14分)海洋是一个巨大的资源宝库。海盐应用很早,现在是氯碱工业的原料。
(1)用提纯后的食盐配制20%的NaCl溶液,应选用的仪器有__________(选填序号)。
a. 烧瓶?b. 容量瓶?c. 量筒?d. 胶头滴管
(2)电解饱和食盐水常用隔膜电解槽或离子膜电解槽。图7为阳离子交换膜电解槽(只允许阳离子通过)示意图。

①请判断E为_________极。
②制得的烧碱溶液从_______处(填字母)流出。
③制得的烧碱溶液中往往含有NaCl,检验其中含有Cl―的具体操作是:______________________________________________________________________。
(3)20℃时制得烧碱混合液中,随着NaOH含量的变化,NaCl达到饱和状态时其溶质质量分数的变化曲线如图。现有20℃时,满足曲线B点所示的溶液,可采用______________
方法降低NaCl的含量,达到提纯目的,简述理由_________________________________________________________________。

(4)欲测定某批次烧碱混合液产品(已知密度为ρg・cm―3)中NaOH的含量,可采用的方法是___________。
参考答案:(1)cd(2分)
(2)①阳极(2分)②L(2分)③取样,加入足量硝酸(或过量),再加入AgNO3溶液,有白色沉淀(2分)
(3)蒸发结晶(或加NaOH固体浓缩)(2分)
溶液中NaOH含量越高,NaCl含量越低(如C点,当NaOH为50%时,NaCl降至1%),所以……(2分)
(4)(中和)滴定法(2分)
本题解析:略
本题难度:简单
4、选择题 0.5 mol Na、Mg、Al分别与100 mL 0.5 mol・L-1的盐酸充分反应,下列关于所得气体在同温同压下的体积关系中,正确的是(?)
A.相同
B.铝最多,钠最少
C.铝最多,镁和钠相同
D.钠最多,镁和铝相同
参考答案:D
本题解析:Na、Mg、Al都能与盐酸反应,从给出的量可知三种金属均是过量的,但过量的钠还能与水反应,因此钠产生的H2最多,而Mg和Al产生的H2一样多。
本题难度:简单
5、计算题 有Na2SO4和Na2CO3混合溶液10.0mL,加入足量BaCl2溶液,充分反应后,经过滤、洗涤、烘干,得到白色沉淀1.45g,将沉淀与过量的盐酸反应,得到112mLCO2气体(标况)。求原混合溶液中Na2SO4和Na2CO3的物质的量浓度。(写出必要的计算过程,只有答案没有过程不给分)
参考答案:n(Na2CO3)= n(BaCO3)= n(CO2)=0.112L÷22.4mol/L=5×10-3mol
n(Na2SO4)= n(BaSO4)="[1.45g-" n(BaCO3)・M(BaCO3)] ÷M(BaSO4)
=(1.45g- 5×10-3mol×137g・mol-1)÷233 g・mol-1
?=3.3×10-3mol
c(Na2CO3)= 5×10-3mol÷0.1L="0.05" mol・L-1?(3分)
c(Na2SO4)= 3.3×10-3mol÷0.1L="0.033" mol・L-1?(4分)
(其它合理运算同样给分)
本题解析:略
本题难度:简单
|