微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 恒温下,将16molN2与bmolH2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)?2NH3(g)
(1)若反应进行到某时刻t时,nt(H2)=15mol, nt(NH3)=6mol,则b的值为______.
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%.计算平衡时:
①原混合气体与平衡混合气体的总物质的量之比______(写出最简整数比,下同)
②达到平衡时,N2和H2的转化率之比a(N2):a(H2)______
③平衡混合气体中,n(N2):n(H2):n(NH3)______.
参考答案:(1)根据方程式计算:
N2(g)+3H2(g)?2NH3(g)
起始(mol):16molb 0
转化(mol):3mol9mol 6mol
t时刻(mol):15mol6mol
所以b-9=15,则b=24,
故答案为:24;
(2)反应达平衡时,混合气体为716.8L22.4L/mol=32mol,其中NH3的物质的量为32mol×25%=8mol,
①利用差量法计算:
N2 (g)+3H2(g)?2NH3(g),物质的量减少△n
1mol 3mol 2mol 2mol
转化:4mol 12mol 8mol 8mol
故原混合气体为:32mol+8mol=40mol,
则原混合气体与平衡混合气体的物质的量之比n(始):n(平)=40mol:32mol=5:4,
答:原混合气体与平衡混合气体的总物质的量之比为5:4;
②反应转化的氮气物质的量为4mol,转化率为:4mol16mol×100%=25%,
转化的氢气物质的量为12mol,转化率为:12mol24mol×100%=50%,
达到平衡时,N2和H2的转化率之比a(N2):a(H2)=25%:50%=1:2,
答:达到平衡时,N2和H2的转化率之比a(N2):a(H2)为1:2;
③平衡混合气的组成为:N2为16mol-4mol=12 mol,NH3为8 mol,H2为32mol-12mol-8mol=12mol,
平衡混合气体中,n(N2):n(H2):n(NH3)=12mol:12mol:8mol=3:3:2,
答:平衡混合气体中,n(N2):n(H2):n(NH3)为3:3:2.
本题解析:
本题难度:一般
2、填空题 (14分)随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)?△H=-574kJ・mol?-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)?△H=-1160kJ・mol-1
则甲烷直接将NO2还原为N2的热化学方程式为?。
(2)全钒氧化还原液流电池,是目前发展势头强劲的优秀绿色环保储能电池。
其电池总反应为:
V3++VO2++H2O VO2++ 2H++V2+。
VO2++ 2H++V2+。
充电过程中,H+向?迁移(填“阴极区”或“阳极区”)。充电时阴极反应式为?。
(3)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g) N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。
该反应的化学平衡常数表达式为K=?。
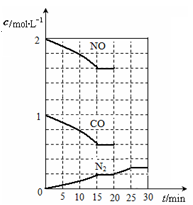
若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如上图所示。若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将?移动(填“向左”、 “向右”或“不”)。
20min时,若改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件
可能是?(填序号)。
①加入催化剂 ?②降低温度 ?③缩小容器体积 ?④增加CO2的量
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为?。
参考答案:(14分)
(1)CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)?△H=-867kJ・mol-1?(2分)
(2)阴极区? V3++e-=V2+?(每空2分)
(3)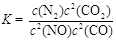 ?不?②?(每空2分)
?不?②?(每空2分)
(4)2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42-+ 4H+?(2分)
本题解析:略
本题难度:一般
3、填空题 (12分)在不同温度下,反应CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数K如下表:
CO(g)+H2O(g)的平衡常数K如下表:
温度/℃
| 700
| 800
| 850
| 1000
| 1200
|
平衡常数K
| 2.6
| 1.7
| 1
| 0.9
| 0.6
|
(1)该反应的△H?0。(填“>”、“=”或“<”)。若到达平衡后升高温度,则CO2的转化率将?,正反应速率?(填“增大”、“减小”或“不变”)。
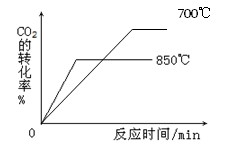
(2)850℃时发生上述反应,CO2的转化率随时间变化如图所示。其他条件相同时,请在下图中画出700℃时CO2的转化率随时间变化的示意图(注明必要的标示)。
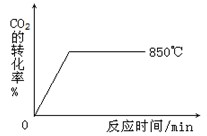
(3)在850℃时发生上述反应,以下表中的物质的量投入恒容反应器,其中向正方向移动的组是?(填代号),平衡后与C中各物质的百分含量相等的组有__________(填代号 )
?
| A
| B
| C
| D
| E
|
n(CO2)[
| 3
| 1
| 0
| 1
| 1
|
n(H2)
| 2
| 1
| 0
| 1
| 2
|
n(CO)
| 1
| 2
| 3
| 0.5
| 3
|
n(H2O)
| 5
| 2
| 3
| 0.5
| 1
|
(4) 850℃时,在1L的密闭容器中分别充入2mol的CO2和H2,计算反应到达平衡时CO的物质的量浓度。(写出计算过程)
参考答案:(1)<,减小,增大(各1分)
(2)如下图(2分)(标注及拐点要明确)
(3)AD? BD(每空2分)
(4)?(5分)解:设平衡时CO的浓度为x
CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
起始浓度(mol・L-1)? 2? 2? 0? 0
转化浓度(mol・L-1)?x?x?x? x
平衡浓度(mol・L-1)(2-x)(2-x)?x? x?(2分)
则:K=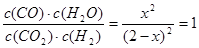 ?(1分)
?(1分)
解得:x=1?即平衡时c(CO) =1 mol・L-1(2分)
本题解析:(1)反应CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数K=
CO(g)+H2O(g)的平衡常数K=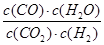 ,随温度升高而减小,说明平衡左移,正反应是放热反应,该反应的△H<0。若到达平衡后升高温度,则CO2的转化率将减小,正逆反应速率均增大。
,随温度升高而减小,说明平衡左移,正反应是放热反应,该反应的△H<0。若到达平衡后升高温度,则CO2的转化率将减小,正逆反应速率均增大。
(2)注意两点:一是温度越高,反应速率越大,越先达到平衡;再有降低温度,则CO2的转化率将增大。
(3)850℃时K=1,所以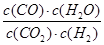 <1时,AD符合题意。
<1时,AD符合题意。
CO2(g)+H2(g) CO(g)+H2O(g)属于两边气体系数相等的可逆反应,依据等效平衡的判断标准可知,只需按照系数比转换为半边,反应物的物质的量比例相同即可,故答案为BD
CO(g)+H2O(g)属于两边气体系数相等的可逆反应,依据等效平衡的判断标准可知,只需按照系数比转换为半边,反应物的物质的量比例相同即可,故答案为BD
(4)见答案
本题难度:一般
4、填空题 在一定温度下,将2molA和2molB两种气体混合放入体积为2L的密闭刚性容器中,发生如下反应: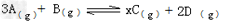 ?
?
2min末反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol/L
请回答: ?
(1)x的值为_______?
(2)A的转化率为α(A)%=______________ ?
(3)此温度下该反应的平衡常数K=___________
参考答案:(1)x=2?
(2)α(A)%=60%
(3)0.5
本题解析:
本题难度:一般
5、选择题 下图为装有活塞的密闭容器,内盛22.4 mL一氧化氮。若通入11.2 mL氧气(气体体积均在标准状况下测定)保持温度、压强不变,则容器内气体的密度(? )
A.等于1.369 g/L
B.等于2.054 g/L
C.在1.369 g/L和2.054 mol/L之间
D.大于2.054 g/L
参考答案:D
本题解析:标准状况下,22.4 mL一氧化氮的物质的量为0.001mol;11.2 mL氧气的物质的量为0.0005mol;由方程式2NO+O2=2NO2可知,两气体恰好完全反应生成0.01molNO2气体;气体物质的量的减少,为保持压强不变,气体体积减小,又因为二氧化氮气体存在如下可逆反应: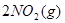 ?
? ,则可得容器内气体的密度大于2.054 g/L
,则可得容器内气体的密度大于2.054 g/L
本题难度:一般