微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 依据元素周期表及元素周期律,下列推断正确的是
A.同一周期元素的原子,半径越小越容易失去电子
B.ⅠA族元素的金属性比ⅡA族元素的金属性强
C.若M+和R2-的核外电子层结构相同,则原子序数R>M
D.主族元素的最高正化合价等于该元素原子的最外层电子数
参考答案:D
本题解析:A.同一周期元素的原子,从左到右半径越来越小,失电能力越来越弱,错误;B.同一周期相比ⅠA族元素的金属性比ⅡA族元素的金属性强,错误;C.若M+和R2-的核外电子层结构相同,则原子序数应该是M>R,错误;D.主族元素的最高正化合价等于该元素原子的最外层电子数,正确;
本题难度:一般
2、填空题 (12分)有A、B、C、D四种元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B 元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质,C为原子核内有12个中子的二价金属,当2 .4克C与足量热水反应时,在标准状况下放出气体2.24L,D的M层上7个电子。(①②③每空1分)
①写出A~D元素符号:A____,B_____,C_____,D_____
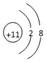
②写出A的原子结构示意图:?B的离子结构示意图::?
D在周期表的位置:??C和D所形成的化合物的电子式?
③分别写出B 、D的最高价氧化物的水化物的化学式______ ,______
④比较D的气态氢化物与H2S和HF的稳定性:(2分)
?
参考答案:①A: O? B: Na? C: Mg? D: Cl ?②?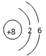 、
、
第三周期第ⅦA、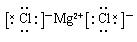
③ NaOH;HClO4?④ HCl>H2S; HCl<HF
本题解析:A元素形成的-2价阴离子比氦原子的核外电子数多8个,说明该负2价阴离子是含有10个电子,则A是氧元素。氧化物为淡黄色固体的是过氧化钠,所以B是Na元素。M层上7个电子的元素是氯元素,即D是Cl。氢气是0.1mol,转移电子0.2mol,所以2.4gC的物质的量是0.1mol,因此C的相对原子质量是24,C原子中含有12个中子,所以质子数是24-12=12,即C是镁元素。
本题难度:一般
3、选择题 具有下列外围电子排布式的基态原子中,最容易形成离子的是:
A.3s23p1
B.2s22p2
C.3s2
D.4s24p3
参考答案:C
本题解析:A.Al B.C C.Mg? D.P
元素周期表位置:
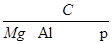 ,金属镁最活泼,最易形成离子。
,金属镁最活泼,最易形成离子。
本题难度:简单
4、选择题 下列各项比较中,不正确的是
A.原子半径:Na<Mg<Al
B.与酸反应放出氢气的剧烈程度:K<Na<Li
C.氧化性:Si>N>O
D.气态氢化物的稳定性:HF>HCl>H2S
参考答案:ABC
本题解析:熟悉元素周期律的规律即可;
本题难度:一般
5、选择题 下列各组微粒半径(R)之比大于1的是?
A.R(Mg)/R(Na)
B.R(P)/R(Cl)
C.R(Al3+)/R(Na+)
D.R(K)/R(Br)
参考答案:B、D
本题解析:同周期元素(主族),从左到右随着核电荷递增,原子半径、阳离子半径或阴离子半径都依次减小。钠和镁都位于元素周期表第3周期,钠在镁的左边,钠原子半径大于镁原子,R(Mg)/R(Na)小于1,A错。磷和氯都位于第3周期,磷在氯左边,磷的原子半径大于氯,R(P)/R(Cl)大于1,B对。钠和铝都失去外层电子成为阳离子,都具有两个电子层,铝的核电荷数大于钠。铝对核外电子吸引力大,铝离子的半径小于钠离子,它们的半径比值小于1,C错。钾和溴都位于第4周期,都是主族元素,钾的原子半径大于溴,两原子半径比大于1,D对。
本题难度:一般