��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� A��B��C��DΪ��ѧ��ѧ���������ʣ����Ǽ�ķ�Ӧ��ϵ��ͼ��ʾ��
��1����A�ǿ�����ǿ�B�����Σ�D������ϡ���ᣬ��B�Ļ�ѧʽ______���йط�Ӧ�Ļ�ѧ����ʽΪ______��
��2����B�����Σ�D�ȿ����������ֿ�����NaOH��Һ����A��NaHCO3ʱ���÷�Ӧ�����ӷ���ʽΪ______��
��3����A��̼���ƣ�CaC2����A��B����Һ��Ӧʱֻ��������C��CaCO3��ˮ��C��ȼ����Ϊ1300kJ?mol-1����B�Ļ�ѧʽΪ______��Cȼ�յ��Ȼ�ѧ����ʽΪ______��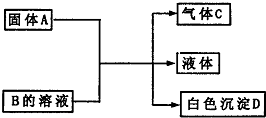
�ο��𰸣���1��ǿ������ι��ȷŰ�������AΪǿ�����BΪ��Σ�����D������ϡ���ᣬ����DΪ���ᱵ����BΪ����泥�AΪ�������������߷�Ӧ����ʽΪ��
Ba��OH��2+��NH4��SO4�TBaSO4+2NH3��+2H2O��
�ʴ�Ϊ����NH4��SO4��Ba��OH��2+��NH4��SO4�TBaSO4+2NH3��+2H2O��
��2��D�ȿ����������ֿ�����NaOH��Һ������֪DΪ����������������A��NaHCO3ʱ��BӦ��Al3+�����߷���˫ˮ�ⷴӦ��
Al3++3HCO3-�TAl��OH��3��+3CO2����
�ʴ�Ϊ��Al3++3HCO3-�TAl��OH��3��+3CO2����
��3����A��̼���ƣ�CaC2����̼���ƣ�CaC2����ˮ��Ӧ�����������ƺ���Ȳ���壨C�����������ƺ�B��Ӧ����̼��ƺ�ˮ�����������غ��֪BΪ̼����ƣ���ѧʽΪ��Ca��HCO3��2��������Ȳ��ȼ���ȿ�д����Ȳȼ�յ��Ȼ�ѧ����ʽ��
C2H2��g��+5/2O2?��g���T2CO2��g��+H2O��l����H=-1300?KJ/mol��
�ʴ�Ϊ��Ca��HCO3��2��C2H2��g��+5/2O2?��g���T2CO2��g��+H2O��l����H=-1300?KJ/mol��
���������
�����Ѷȣ�һ��
2��ѡ���� ���й�ϵͼ�У�A��һ�����Σ�B����̬�⻯�C�ǵ��ʣ�F��ǿ�ᡣ��X������ǿ�ỹ��ǿ��ʱ��������ת����ϵ(������Ӧ���P��Ӧ��������������ȥ)����X��ǿ��ʱ����B�ĸ�Cl2��Ӧ����C���⣬��һ�����������Ρ�����˵���в���ȷ����

[? ]
A����X��ǿ��ʱ��A��B��C��D��E��F�о���ͬһ��Ԫ�أ�F������
B����X��ǿ��ʱ��A��B��C��D��E��F�о���ͬһ��Ԫ�أ�F��
C��B��Cl2�����ķ�Ӧ��������ԭ��Ӧ
D����X��ǿ��ʱ��C�ڳ���������̬����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3���ƶ��� ��ͼ��ʾ��������֮���ת����ϵ������A��B��Ϊ��ɫ��ĩ��BΪ�ǽ������ʣ�CΪ��ɫ�����壬DΪ�������ʣ�E�Ǻ���ɫ���壬G�Ǿ���Ư���Ե����壬H��ˮ��Һ����ɫ����ش���������

(1)A�Ļ�ѧʽ��____________��C�ĵ���ʽ��___________��Y��������___________��
(2)��Ӧ�ٵĻ�ѧ����ʽΪ______________________��
(3)ʵ���Ҳⶨ����E����Է�������ʱ���õ���ʵ��ֵ���DZ�����ֵƫ����ԭ����(�û�ѧ����ʽ��ʾ)______________________��
(4)19.2g��D��������һ��Ũ��X����Һ��Ӧ�������õ�������_______L O2(��״����)��ϣ�ǡ���ܱ�ˮ��ȫ���ա�
�ο��𰸣�(1)CuO������ʽ���ԡ���Ũ����
(2)C��4HNO3(Ũ) ===CO2����4NO2����2H2O
(3)2NO2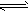 N2O4
N2O4
(4)3.36L
���������
�����Ѷȣ�һ��
4������� ʳ�����ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϡ�
(1)��ʳ�γ���������Ca2����Mg2����SO42�����������ӣ�ʵ�����ᴿNaCl���������£�
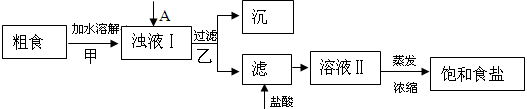
�ṩ���Լ�������Na2CO3��Һ?����K2CO3��Һ? NaOH��Һ? BaCl2��Һ? Ba(NO3)2��Һ
(1)������ȥ��Һ���е�Ca2����Mg2����SO42����ѡ��A���������Լ������μ�˳������Ϊ?(ֻ�ѧʽ)��������Һ��SO42��������ȫ�IJ���Ϊ?��
�ڼ������Ŀ����(�����ӷ���ʽ��ʾ)?��
�����������У��ס����������̾�Ҫ�õ��������������������÷ֱ��Ǽ�?����?��
(2)��ҵ���ö��Ե缫��ⱥ��ʳ��ˮ����ȡ���ᣬд����ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ?������ֽ������ʳ��ˮ��������ķ�����?��
�ο��𰸣���1����BaCl2��NaOH ��Na2CO3��NaOH��BaCl2��Na2CO3
�Դ�Ƭ�̣�������������ϣ��ϲ������Һ�����ϲ���Һ�м����μ��Ȼ�����Һ���������ɣ��������ȫ��
��OH����H��=H2O? CO32����2H��=H2O��CO2��
�۽�������
��2��2NaCl��2H2O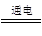 2NaOH��H2����Cl2��
2NaOH��H2����Cl2��
��ʪ�����ɫʯ����ֽ���������������У���ֽ�ȱ�죬����ɫ��֤������������(����ʪ���KI-������ֽ���������������У���ֽ����ɫ)
�����������1������Ca2+��Na2CO3��Һ������Mg2+��NaOH��Һ������SO42-��BaCl2��Һ����Ҫע������Լ���������ҹ������Լ��������������ȥ�������Լ��μӵ�˳����BaCl2��NaOH ��Na2CO3��NaOH�� BaCl2��Na2CO3������SO42-������ȫ�IJ�������Ϊ����Һ���ã����ϲ���Һ�м����μ��Ȼ�����Һ���������ɣ�˵��SO42-��ȫ��������Һ�м�����������dz�ȥ������CO32-��OH-���ܽ�ʱ�ò��������裬�ӿ��ܽ��ٶȡ�����ʱ�ò�����������
��2����ⱥ��ʳ��ˮ�����������ơ�������������������������������ʪ�����-KI��ֽ���顣
����������ʱҪע���Լ������˳���������Լ���������������Լ��������������ȥ��
�����Ѷȣ�һ��
5������� ��15�֣�I����ͼת����ϵ�У��������ɫ��Ӧ�ʻ�ɫ��MΪ������Һ�����ʣ���G����Ҫ�Ļ�����Ʒ�ͻ���ԭ�ϣ�����H���ܽ���A����G��HΪ���õ��ͻ����(ͼ�в��ֲ���û���г�)��
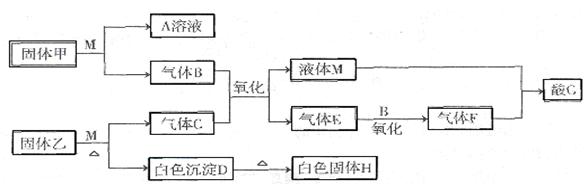
II��ͼ��ʾ����������G�Ĺ�ҵ���̣�
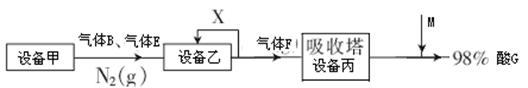
��1�����豸������Ϊ?�����ҵĻ�ѧʽΪ?M���ӵĽṹʽΪ?��
��2������X����Ҫ�ɷ�Ϊ?��
��3��д���豸���г����Ļ�ѧ��Ӧ?��
��4����ɫ����D��G��Һ��Ӧ�����ӷ���ʽΪ?��
��5����2.24 L����״���£�Eͨ��100 mL2 mol/L A��ˮ�� Һ����Һ������Ũ���ɴ�С��˳��Ϊ____________?___��
Һ����Һ������Ũ���ɴ�С��˳��Ϊ____________?___��
��6��������ڹ���H���Ƶ�һ�ֽ��������⻯ѧ����ʽΪ?�����ʱת��2.4mol���ӣ��Ƶý���?g��
�ο��𰸣�
��1���Ӵ��ң�1�֣�?Al2S3?��1�֣�? H����O����H?��1�֣�
��2��SO2��O2��N2��2�֣�
��3��4FeS2 + 11O2 2Fe2O3 + 8SO2��2�֣���������Ҳ���֣�
2Fe2O3 + 8SO2��2�֣���������Ҳ���֣�
��4��Al(OH)3? + 3H+ ="==" Al3+ + 3H2O?��2�֣�
��5��c(Na*)��c(SO32-)��c(OH-)��c(HSO3-)��c(H*)?��2�֣�
��6��2Al2O3 4 Al + 3O2��(ֻҪ��ͨ�������������)��2�֣�?21.6g��2�֣�
4 Al + 3O2��(ֻҪ��ͨ�������������)��2�֣�?21.6g��2�֣�
�����������
�����Ѷȣ�һ��