��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�ܱ������г���һ������N2��H2�����ⶨ��Ӧ��ʼ���2s��������ƽ�����ʣ���(H2)=0.45mol/(L��s)����2sĩNH3��Ũ��Ϊ
A��0.50mol/L
B��0.60mol/L
C��0.45mol/L
D��0.55mol/L
�ο��𰸣�B
������������ݷ�Ӧ�Ļ�ѧ����ʽΪ��N2+3H2 2NH3�ɵ� ��V(H2)��V(NH3 )="3:2" ��V(NH3 )=��2�M3��V(H2)= ��2�M3����0.45mol/(L��s)="0.30" mol/(L��s)������2sĩNH3��Ũ��Ϊ��C(NH3)="��t" ��V(NH3 )="2s��=0.30" mol/(L��s)="0.60" mol/L��ѡ��Ϊ��B��
2NH3�ɵ� ��V(H2)��V(NH3 )="3:2" ��V(NH3 )=��2�M3��V(H2)= ��2�M3����0.45mol/(L��s)="0.30" mol/(L��s)������2sĩNH3��Ũ��Ϊ��C(NH3)="��t" ��V(NH3 )="2s��=0.30" mol/(L��s)="0.60" mol/L��ѡ��Ϊ��B��
�����Ѷȣ�һ��
2��ʵ���� (10��)���о�֪Cu2����H2O2�ֽ�Ҳ���д����ã�Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч����ij�о�С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣�ش�������⣺
(1) ���Է�������ͼ��ͨ���۲�____________________________________�����ԱȽϵó����ۡ���ͬѧ�����FeCl3��ΪFe2(SO4)3��Ϊ��������������____________________________________________________________________��
д��H2O2�ڶ������������·�����Ӧ�Ļ�ѧ����ʽ
____________________________________________________________________��
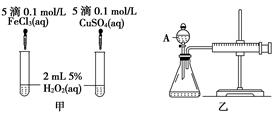
(2) ������������ͼ����ʾ��ʵ��ʱ��������40mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԡ�ͼ������A������Ϊ________��ʵ������Ҫ������������___________________________________________________________��
�����װ�������Եķ�����
____________________________________________________________________��
(3) 0.6 mol X�����0.6 mol Y��������2 L�ܱ������У��������·�Ӧ��
2X(g)��Y(g)===nZ(g)��2W(g)�� 2 minĩ����0.2 mol W���������Z�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.1 mol��(L��min)����ǰ2 min�ڣ���X�����ʵ���Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ________��2 minĩʱY�����ʵ���Ũ��Ϊ________����ѧ����ʽ�У�Z�Ļ�ѧ������n��________��
(4) ��һ���¶��£���Ӧ��2A(s)��2B(g) 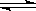 ?C(g)��D(g)�ں��������н��У�����˵���÷�Ӧ�Ѿ��ﵽƽ�����________
?C(g)��D(g)�ں��������н��У�����˵���÷�Ӧ�Ѿ��ﵽƽ�����________
A�������ڵ�ѹǿ����ʱ����仯
B����������ܶȲ�����ʱ����仯
C��A���������ٸı�
D��ƽ���������ƽ����Է����������ٸı�
�ο��𰸣�(1)��Ӧ�������ݿ�����������������ͬ���ų������ӵĸ���
(2)��Һ©�����ռ�40mL��������Ҫ��ʱ�䡡�ر�A�ϵIJ�������������Ͳ�Ļ�������(���ƽ�)һ�κ��ɿ��������ܻص�ԭ����λ��˵������������(�����𰸺���Ҳ����)
(3)v(X)��v(W)��0.05 mol��L��1��min��1�� 0.25 mol/L��4��
(4)A
�����������1�������IJ�ͬ������Ӧ���ʵIJ�ͬ�����Ը��ݷ�Ӧ�в������ݵĿ��������Է��������Ĵ�Ч����Ϊ����ʵ����пɱ��ԣ�Ӧ��ʹ��Һ�е�������Ҳ��ͬ�����������ų������Ӳ�ͬ������ɵĸ��š�
��2������۷���A�Ƿ�Һ©�����ռ���ͬ������������Ҫ��������ʱ��ij��̡�����װ�õ��Ҳ��Ǵ��л�������Ͳ�����Լ�����������ʱ�������ô�ͳ�ķ������飬��ȷ�ķ����ǹر�A�ϵIJ�������������Ͳ�Ļ�������(���ƽ�)һ�κ��ɿ��������ܻص�ԭ����λ��˵�����������ã�����©����
��3����Z�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.1 mol��(L��min)���������Z�����ʵ�����0.1 mol��(L��min)��2L��2min=0.4mol��ͬʱ����W��0.2mol����Ϊ���ʵı仯��֮������Ӧ�Ļ�ѧ������֮�ȣ�����n����4.����Ϊ���ʵ����ı仯������Ӧ�Ļ�ѧ�������dz����ȵģ���������֮��Ӧ������Ӧ�Ļ�ѧ������֮�ȣ�����X�����ʵ���Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ҳ��0.05 mol��(L��min)������0.2molW���ͱ�Ȼ����0.1molY����ʣ��Y��0.5mol������2 minĩʱY�����ʵ���Ũ��Ϊ0.25mol/L��
��4����Ϊ��Ӧǰ�����������Dz���ģ������ڷ�Ӧ������ѹǿʼ���Dz���ģ�A����ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ݻ����䣬��������������DZ仯�ģ����Ե���������ܶȲ�����ʱ����仯ʱ������˵���ﵽƽ��״̬��A���������ٸı䣬˵�����淴Ӧ������ȣ����ѡ��C��ȷ����������ƽ����Է��������ǻ�����������ͻ���������ʵ����ı�ֵ������������ʵ������䣬�������DZ仯�ģ���˵�ƽ���������ƽ����Է����������ٸı�ʱ����˵���Ѿ��ﵽƽ��״̬��
�����Ѷȣ�һ��
3��ѡ���� ��mA+nB
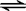
pC�ķ�Ӧ��m��n��pΪ�����ʵĻ�ѧ���������ֲ��Cÿ��������aMol/L��Bÿ���Ӽ�С1.5a?mol/L��Aÿ���Ӽ���0.5a?mol/L����m��n��pΪ��������
A��2��3��2
B��2��2��3
C��1��3��2
D��3��1��2
�ο��𰸣�Ũ�ȵı仯����ʱ��ı�ֵΪ��Ӧ���ʣ�����A��B��C�ķ�Ӧ���ʷֱ���0.5a?mol/Lmin��.1.5a?mol/L��min��
amol/L��min����ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ����������֮�ȣ�����A��B��C�ļ�����֮��=0.5a?mol/Lmin
��1.5a?mol/L��min��amol/L��min��=1��3��2����ѡC
���������
�����Ѷȣ�һ��
4��ѡ���� ����Ƭ��ϡ������ȡ����ʱ�����д�ʩ��ʹ�����������ʼ������ǣ�������
A��ʹ�ø�ϡ��������Һ
B������
C���μ�����CuSO4��Һ
D��������Ƭ����������
�ο��𰸣�A��ʹ�ø�ϡ��������Һ����Ӧ��Ũ�ȼ�С����Ӧ���ʽ��ͣ���Aѡ��
B�����ȣ��¶����ߣ���Ӧ��������B��ѡ��
C���μ�����CuSO4��Һ�����û���ͭ���γ�ԭ��ط�Ӧ����Ӧ��������C��ѡ��
D���������ۣ��Ӵ������Ӧ��������D��ѡ��
��ѡA��
���������
�����Ѷȣ���
5��ѡ���� ����������ȷ����
A���ú˴Ź��������Լ���lһ������2һ�����
B�����ڿ��淴ӦN2(g)+3H2(g)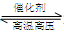 2NH3(g)��������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
2NH3(g)��������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
C����AlCl3��Һ��NaAl02��Һ�ֱ����ɺ����գ����ù�������ΪAl2O3
D��BaS04��ͬ���ʵ���Ũ�ȵ������ƺ���������Һ�е��ܽ����ͬ
�ο��𰸣�A
���������A��ǰ���������⡢�����������⣬��ȷ
B��������Ũ��ֻ�����ӵ�λ����ڻ���Ӹ�����������Ӱٷ�����û�иı䣬����ȷ
C�����ù����Al2O3�⣬����NaCl������ȷ
D������Һ����������ӵ�Ũ�Ȳ�ͬ���Գ����ܽ�ƽ������Ƴ̶Ȳ���ȣ���BaS04���ܽ�Ȳ���ͬ���ų�
��ΪA
�����Ѷȣ�һ��