微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一些科学家采用高质子导电性的SCY陶瓷 (能传递H+),实现了氨的电化学合成。该过程N2和H2的转 化率远高于现在工业上使用的氨合成法。对于电化学合成氨的有关叙述正确的是
? [? ]
A.N2在阴极上被氧化
B.可选用铁作为阳极 材料
C.阳极的电极反应式是N2+6e-+6H+==2NH3
D.该过程的总反应式是N2+3H2 2NH3
2NH3
参考答案:D
本题解析:
本题难度:一般
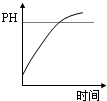
2、选择题 用石墨作电极电解AlCl3溶液时,下列图象合理的是( )
A.

B.
C.

D.
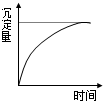
参考答案:中间的虚线pH=7,溶液pH之所以不会大于7,可能情况有两种:①电解生成的氯气溶于水变成盐酸和次氯酸,使得溶液呈酸性;②电解产生的OH-会和溶液中的铝离子反应生成氢氧化铝沉淀,不会有多余的氢氧根,所以溶液不会呈碱性,所以A是正确的,电解的初期会有沉淀生成,后期相当于电解水,不会有多余的氢氧根,所以沉淀量不会改变,所以D正确.
故选AD.
本题解析:
本题难度:简单
3、填空题 A、B、C三种强电解质,它们在水中电离出的离子为Na+、Ag+、NO3-、SO42-、Cl-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:
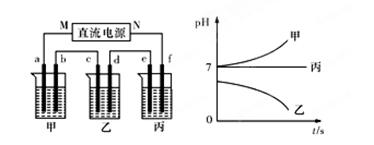
(1)M为电源的 极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为 ?、 ?(填写化学式)。
(2)计算电极f上生成的气体在标准状况下体积为 ?L。
(3)写出乙烧杯中的电解反应方程式:?。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为 ?。
参考答案:(1)负? NaCl? AgNO3?(2)0.56L (3)4AgNO3+2H2O 4Ag+4HNO3+O2↑ (4)12
4Ag+4HNO3+O2↑ (4)12
本题解析:(1)经过一段时间后,测得乙烧杯中c电极质量增加了10.8克,这说明c电极是阴极,则M是负极,N是正极,f是阳极,e是阴极,d是阴极,b是阴极,a是阴极。乙中电解后pH降低,说明酸性增强,因此电解液应该是硝酸银溶液。甲中pH升高,说明碱性增强,因此电解液应该是氯化钠。丙中pH不变,则相当于是电解水,因此电解液是硫酸钠或硝酸钠。
(2)c电极析出的单质银,物质的量=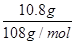 =0.1mol,转移电子的物质的量是0.1mol。f电极是阳极,溶液中的OH-放电,4OH--4e-=2H2O+O2↑。则根据电子转移守恒可知,生成氧气的物质的量是
=0.1mol,转移电子的物质的量是0.1mol。f电极是阳极,溶液中的OH-放电,4OH--4e-=2H2O+O2↑。则根据电子转移守恒可知,生成氧气的物质的量是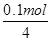 =0.025mol,标准状况下的体积=0.025mol×22.4L/mol=0.56L。
=0.025mol,标准状况下的体积=0.025mol×22.4L/mol=0.56L。
(3)乙中电解质是硝酸银溶液,则电解反应方程式为4AgNO3+2H2O 4Ag+4HNO3+O2↑。
4Ag+4HNO3+O2↑。
(4)甲中电解质是氯化钠,电解的方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,根据电子守恒可知,反应中生成氢氧化钠的物质的量是0.1mol,其浓度是
2NaOH+H2↑+Cl2↑,根据电子守恒可知,反应中生成氢氧化钠的物质的量是0.1mol,其浓度是 =0.01mol/L,则pH=12。
=0.01mol/L,则pH=12。
本题难度:一般
4、选择题 用石墨作电极,电解下列物质的溶液,其实质不是电解水的是( )
A.NaNO3
B.NaOH
C.Na2SO4
D.NaCl
参考答案:D
本题解析:四个选项中阳离子相同,放电顺序为H+(水)>Na+,阴离子的放电顺序为Cl->OH->含氧酸根,因此在阳极A、B、C三项均为OH-放电;而D项在阳极上为Cl-放电,故D项不是电解水。
本题难度:一般
5、选择题 质量均为100 g的Cu作电极,电解AgNO3溶液。稍电解一段时间后,两电极的质量相差28 g,此时两电极的质量分别为 (?)
A.阳极100 g,阴极128 g
B.阳极93.6 g,阴极121.6 g
C.阳极91.0 g,阴极119.0 g
D.阳极86.0 g,阴极114.0 g
参考答案:B
本题解析:阳极Cu-2e-=Cu2+;阴极Ag++e-=Ag;设转移xmol电子,阳极减少32xg,阴极增加108xg,相差32x+108x=28,x=0.2。故答案为B
本题难度:一般