| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《电解池原理》考点强化练习(2017年押题版)(八)
参考答案:D 本题解析:A.若断开K1关闭K2则构成电解池,X、Y均为石墨,Z是NaCl溶液,X 是阳极,氯离子放电生成氯气,错误;B.若断开K1关闭K2则构成电解池,X是阳极,电极材料为粗铜,Y是精铜,Z是CuSO4溶液,才可用于铜的精炼,错误;C.若断开K2关闭K1则构成原电池,X是Cu,Y是Fe,Z是含有空气的海水,铁比铜活泼做负极,受到腐蚀,该装置不能用于保护Fe,错误;D.若断开K2关闭K1则构成原电池,X是Cu,Y是Zn,Z是稀H2SO4,锌比铜活泼,则在X极有气泡生成,正确;选D。 本题难度:一般 4、选择题 用Pt电极电解含有0.1 mol Cu2+和0.1 mol X3+的溶液,阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n(mol)的关系如图所示。则离子的氧化能力由大到小排列正确的是 参考答案:D 本题解析: 本题难度:一般 5、填空题 (10分)某校化学小组的同学以碳棒为电极电解氯化铜溶液时发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的附着物,设计了如下过程:
(1)提出假设:①红色物质一定有铜,还可能有Cu2O;②根据以上资料,白色物质化学式可能为 。 (2)实验验证: 取电解CuCl2溶液后的阴极碳棒附着物,洗涤、干燥,连接下列装置进行实验,验证阴极产物。 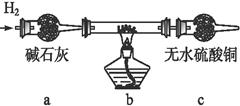 实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色。 ①碳棒上的红色物质有无Cu2O? (填“有”或“无”),请简要说明的理由: ; ②在c装置后将气体通入硝酸银溶液中,若出现白色沉淀,可说明提出假设②中的白色物质一定存在,写出装置b中发生反应的化学方程式: 。 (3) 由以上实验分析可知:电解CuCl2溶液的阴极上发生的电极反应式为Cu2++2e-  Cu和 。 Cu和 。 参考答案:(10分)(1)CuCl (2分) 本题解析:(1)根据表中提供的信息可知,只有CuCl是白色不溶于水的固体,所以白色物质的化学式可能是CuCl; 本题难度:困难 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《金属及其化.. | |