微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A、B是短周期元素,最外层电子排布式分别为msx,nsxnpx+1。A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该化合物的相对分子质量是
A..38? B.55? C.100? D.135
参考答案:C
本题解析:由nsxnpx+1知x=2,即AB两元素的最外层电子排布式为:ms2、ns2np3;由题意知两元素分别为活泼的金属Mg和非金属N
Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
本题难度:一般
2、选择题 下列结论正确的是(?)
①粒子半径:K+>Al3+>S2->Cl-?②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-?④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO?⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
A.只有②⑤⑦
B.②⑥⑦
C.②④⑤⑥⑦
D.②④⑥
参考答案:C
本题解析:①原子核外电子排布相同的离子,核电核数越大,半径越大,离子的原子核外电子层数越多,半径越大;②元素的非金属性越强,对应的氢化物越稳定;③元素的非金属性越强,对应阴离子的还原性越弱;④元素的非金属性越强,对应单质的氧化性越强;⑤元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;⑥同周期元素从左到右元素的非金属性逐渐增强,同主族元素从上到下元素的非金属性逐渐减弱;⑦同周期元素从左到右元素的逐渐减弱,同主族元素从上到下元素的金属性逐渐增强。
本题难度:一般
3、选择题 科研人员最近发现放射性同位素钬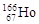 可有效地治疗肝癌。该同位素原子核内中子数与质子数之差为?
可有效地治疗肝癌。该同位素原子核内中子数与质子数之差为?
A.32
B. 99
C.166
D.233
参考答案:A
本题解析:67166Ho中质子数为67,质量数为166,中子数=质量数-质子数=166-67=99,由题意知核外电子数等于核电荷数为
67,该同位素原子核内的中子数与质子数之差为:99-67=32。
故选A。
点评:本题考查质子数、中子数、核外电子数及其相互联系,通过回答本题要知道在原子里:质子数=电子数=核电荷数;相对原子质量=质子数+中子数。
本题难度:简单
4、选择题 下列说法中正确的是
A.3p2表示3p能级有两个轨道
B.处于最低能量的原子叫基态原子
C.同一原子中,1s、2p、4p电子能量逐渐降低
D.同一原子中,2p.3p.4p能级的轨道数依次增多
参考答案:B
本题解析:略
本题难度:一般
5、填空题 (15分)
现有A、B、C、D四种常见的短周期主族元素,其原子序数依次增大.其中A、B是同周期相邻元素,且A单质及其氢化物是重要的工业生产原料;C、D是同周期元素,且在该周期中,分别为原子半径最大和最小的元素,C、D最外层电子数之和与B的原子序数相等,回答下列问题:
(1)B元素的名称为?,C元素在周期表中位于第?周期第?族.
(2)工业上由A单质合成其氢化物的化学反应方程式为:?.
(3)当今工业电解CD饱和水溶液的装置名称是?,阳极电极反应式为?,溶液的pH将?(填“增大”、“减小”或“不变”),若有1mol电子转移,生成气体体积之和是??L(标准状况下).
参考答案:
(1)氧(2分)?三(1分)? IA(1分)
(2)N2+3H2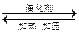 2NH3(3分)(不写可逆号及反应条件扣2分)
2NH3(3分)(不写可逆号及反应条件扣2分)
(3)离子交换膜电解槽(2分)2Cl―-2e―=Cl2↑(2分),增大(2分),22.4(2分)
本题解析:略
本题难度:简单