微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0
C.钢铁在潮湿的空气中会形成原电池而被腐蚀,其正极反应为:O2 + 2H2O + 4e-=4OH-
D.原子结合成分子的过程一定释放出能量
参考答案:A
本题解析:A 错误,铅蓄电池在放电过程中,负极铅会失去电子,得到的铅离子和硫酸根离子结合生成硫酸铅沉淀,负极质量增加。
B 正确,C(s)+CO2(g)=2CO(g)是吸热反应。
C 正确,钢铁在潮湿的空气中会发生吸氧腐蚀。
D 正确,原子结合成分子的过程是形成化学键的过程,一定释放出能量。
本题难度:简单
2、填空题 古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重(电化腐蚀)。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,可将土壤中的SO42-还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。
①写出该电化腐蚀的正极反应的电极反应式:?
②文物出土前,铁器表面的腐蚀产物可能有(写化学式)?
参考答案:①SO42-+8e-+ 4H2O=S2-+8OH-;②Fe (OH)2;FeS。
本题解析:根据题意可知,正极:SO42-+8e-+ 4H2O=S2-+8OH- ,负极:Fe-2e-=Fe2+ ,两极产物相遇,生成Fe (OH)2? FeS。
本题难度:简单
3、填空题 (9分)下图所示水槽中试管内有一枚铁钉,放置数天后观察:
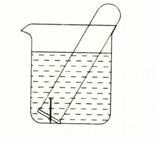
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于?腐蚀。
(2)若试管内液面上升,则原溶液呈?性,发生?腐蚀,正极反应式为?。
(3)若试管内液面下降,则原溶液呈?性,发生?腐蚀,正极反应式为?。
参考答案:(9分)
(1)电化学(2)弱酸性或中;吸氧);O2+2H2O+4e―====4OH―
(3)较强的酸;析氢;2H++2e―===H2 ↑
本题解析:(1)铁钉表面形成无数个微小的铁碳原电池,属于电化学腐蚀;
(2)若试管内液面上升,说明发生了吸氧腐蚀,溶液呈弱碱性,相关方程式:正极:O2+2H2O+4e―====4OH―;负极:Fe? -2e-=Fe2+;
(3)若试管内液面下降,说明发生了析氢腐蚀,溶液呈酸性;相关方程式:正极:2H++2e―===H2 ↑;负极:Fe? -2e-=Fe2+?。
本题难度:一般
4、填空题 (18分)按要求完成下列问题。
⑴.写出铅蓄电池放电时的总反应和两个电极反应及反应类型
放电总反应:?
负极:?(?)反应;?
正极:?(?)反应;
⑵.写出氯碱工业中电解饱和食盐水的总反应和两个电极反应及反应类型
电解总反应:?
阳极:?(?)反应;
阴极:?(?)反应;
⑶.氢氧燃料电池中用KOH做电解质溶液,H2是还原剂,O2是助燃剂,写出正、负两极的电极反应
负极:??正极:?
参考答案:⑴放电总反应(2分):Pb+PbO2+2H2SO4=2PbSO4+2H2O?
负极(2分): Pb+ SO42--2 e-= PbSO4?(氧化)反应;(1分)?
正极(2分): PbO2 +4H++SO42-? + 2 e-= PbSO4 +2H2O (还原)反应;(1分)
⑵电解总反应(2分):( 2NaCl +2H2O? =" 2NaOH" + Cl2↑ + H2↑)
阳极(1分):2Cl-―2e- ="?" Cl2↑?(氧化)反应;(1分)
阴极(1分):2H+ + 2 e- = H2↑或 2H2O + 2 e- = H2↑+ 2OH -?(还原)反应;(1分)
⑶负极(2分):(2H2 + 4 OH -― 4 e-=" 4" H2O ) 正极(2分):( O2+2H2O+ 4e--=" 4" OH -);
本题解析:略
本题难度:一般
5、选择题 铜制品上的铝质铆钉,在潮湿空气中易腐蚀的原因可描述为
[? ]
A.形成原电池,铝作负极
B.形成原电源,铜作负极
C.形成原电池时,电流由铝经导线流向铜
D.铝质铆钉发生了化学腐蚀
参考答案:A
本题解析:
本题难度:简单