��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������ʵ���������ý�����ȷ����
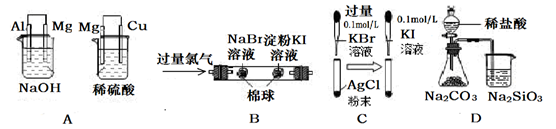
ʵ��
| ʵ������
| ����
|
A
| ����ձ���þ���������ݣ��ұ��ձ���ͭ����������
| ��ԭ�ԣ� Al��Mg��Cu
|
B
| �������Ϊ��ɫ���ұ�����Ϊ��ɫ
| �����ԣ�Cl2��Br2��I2
|
C
| �Թ��а�ɫ�����ȱ䵭��ɫ�����Ϊ��ɫ
| ����ת����ʵ�ʾ��dz����ܽ�ƽ����ƶ�
|
D
| ��ƿ��������������ձ�����Һ�����
| �ǽ����ԣ�Cl��C��Si
|
�ο��𰸣�C
���������A������ձ�����������NaOH��Һ��Ӧ��������������þ���������������ݣ��ұ��ձ��У�þ������ϡ���ᷴӦ��þ��������ͭ��������ͭ���������ݣ�ʵ��������ȷ�������۴��Ƚ�ʱ���õ��Լ���ͬ���ó��˴���Ľ��ۣ�A�����������Ϊ��ɫ����˵�������ԣ�Cl2��Br2�����ұ�����Ϊ��ɫ����ȷ��������KI�����˷�Ӧ���п�����Cl2��KI�����˷�Ӧ��B�������ɫ��������Һ���ټ������KBr��Һ���ٵ���KI����ɫ�����ȱ䵭��ɫ����ɫ��˵����������ת����һ����ƽ���ƶ��Ľ����C�ԣ�Ҫͨ���ȽϷǽ����γɵ��������ǿ�����ȽϷǽ����Ե�ǿ���Ļ���һ��Ҫ�Ƚ���ۺ����������ǿ���������Cl����ۺ����ᣬD����ѡC��
���㣺�����ԡ��ǽ����Ե�ǿ���ıȽ϶ϣ������ܽ�ƽ���Ӧ�á�
�����Ѷȣ�����
2��ѡ���� ������������ȷ���ǣ�������
A�������Ԫ�صĻ����һ������ǿ������
B��������ֻ�������ԣ�������ֻ�л�ԭ��
C��ʧ����Խ�࣬��ԭ��Խǿ
D��ǿ��������ǿ��ԭ����һ���ܷ���������ԭ��Ӧ
�ο��𰸣�A��Ԫ�ر�����������Ҫ�ǿ��õ����������ǽ����Խ�����Ԫ�شﵽ��ʱ�������Զ���ǿ��û�������ԣ���CO2��CԪ�أ�NaOH��NaԪ�أ����ǽ�����ǿ��Ԫ��������γɻ�����Ҳ����������HClO4�����Ժ�������A����
B���������Ӽ������������л�ԭ�ԣ��Ȼ����ܱ������������Ϊ�������������Ȼ���Ļ�ԭ�ԣ���B����
C��ʧ��������ǿ����ԭ��ǿ����ԭ�Ե�ǿ����ʧ���Ӷ���û�й�ϵ����C����
D��������������Ϊ������������Ĥ����������Ӧ������ǿ��������ǿ��ԭ����һ���ܷ���������ԭ��Ӧ����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� ������������������ԭ��Ӧ����2FeCl3+2KI 2KCl+2FeCl2+I2?
2KCl+2FeCl2+I2?
��2Fe+3Cl2 2FeCl3?��2KMnO4 +16HCl
2FeCl3?��2KMnO4 +16HCl 2KCl+2MnCl2+5Cl2��+8H2O����ij��Һ����Fe2+��I-��Cl-���棬Ҫ������ȥI-����Ӱ��Fe2+��Cl-���ɼ�����Լ���
2KCl+2MnCl2+5Cl2��+8H2O����ij��Һ����Fe2+��I-��Cl-���棬Ҫ������ȥI-����Ӱ��Fe2+��Cl-���ɼ�����Լ���
A��KMnO4
B��FeCl3
C��Cl2
D��HCl
�ο��𰸣�B
������������ݢ�KMnO4������Cl-�������ݢ������������������ӡ�����������Ӳ���Ӧ���ܳ�ȥ��
�����Ѷȣ�һ��
4��ѡ���� ���ݱ�����Ϣ�жϣ�����ѡ���ȷ���ǣ�?��
����
| �μӷ�Ӧ������
| ������
|
��
| KMnO4 ��H2O2?��H?2SO4
| K2SO4 ��MnSO4����
|
��
| Cl?2 ��FeBr?2
| FeCl3��FeBr3
|
��
| MnO4��? ����
| Cl2 ��Mn2+? ����
|
?
A���ڢ��鷴Ӧ���������ΪH2O�� O2
B���ڢ��鷴Ӧ��Cl?2 �� FeBr?2�����ʵ���֮��Ϊ1�U2
C���ڢ��鷴Ӧ������1mol Cl2��ת�Ƶ���2mol
D����������ǿ����˳��ΪMnO4-?> Cl2 > Fe3+ > Br2
�ο��𰸣�D
���������������ԭ��Ӧ����Ҫ������Ԫ�صĻ��ϼ���������������ԭ��Ӧ�Ļ�������ͻ������ɽ�������A����Ӧ��KMnO4��MnSO4��MnԪ�ػ��ϼ���+7�۽���Ϊ+2�ۣ���H2O2����Ԫ�ػ��ϼ����ߣ���������������HԪ���غ��֪������ˮ����ȷ��B���������Ϣ֪����Ӧ��ֻ���������ӱ����������ݵ���ת���غ�2n��C12��=n��FeBr2������n��C12����n��FeBr2��=1��2����ȷ��C���������Ϣ֪��MnO4-����Cl-ΪCl2��ClԪ�ػ��ϼ���-1������Ϊ0�ۣ�����1mo1C12ת�Ƶ���Ϊ2mo1����ȷ��D��������������ǿ���������������ԣ��ɢۿ�֪������MnO4-��Cl2���ɢڿ�֪������Cl2��Fe3+���ɢڿ�֪Fe3+��������Br-��������Br2��Fe3+������
�����Ѷȣ�һ��
5��ʵ���� ��10�֣�ijУ��ѧʵ����ȤС���ڡ�̽��±�ص��ʵ������ԡ���ϵ��ʵ���з��֣���������ϡ�Ȼ�������Һ�У�����1��2����ˮ������Һ�ʻ�ɫ��
��1��������⣺Fe3+��Br2��һ���������Ը�ǿ��
��2������
�ټ�ͬѧ��Ϊ�����ԣ�Fe3+>Br2��������ʵ�������Ƿ�����ѧ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ�
���ѧʽ����ͬ�����¡�
����ͬѧ��Ϊ�����ԣ�Br2>Fe3+��������ʵ�������Ƿ�����ѧ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ�___���¡�
3�����ʵ�鲢��֤
��ͬѧΪ��֤��ͬѧ�Ĺ۵㣬ѡ������ijЩ�Լ���Ƴ����ַ�������ʵ�飬��ͨ���۲�ʵ������֤������ͬѧ�Ĺ۵�ȷʵ����ȷ�ġ���ѡ�õ��Լ���
A����̪��Һ
B��CCl4
C����ˮ�ƾ�
D��KSCN��Һ