微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
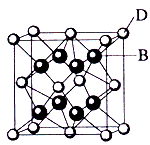
1、填空题 已知A、B、C、D和E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图。 请回答
(1)写出B的电子排布图____________,C的元素符号是____________,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是____________;
(2)E属元素周期表中第______周期,第______族的元素,其元素名称是____________,它的+2价离子的电子排布式为_____________________
(3)写出C的单质与水反应的化学方程式________________________;
(4)如图所示,D跟B形成的离子化合物的化学式为____________;鉴别该离子化合物是否为晶体,最可靠的科学方法是________________________,该离子化合物晶体的密度为ag・cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是____________cm3(只要求列出算式)。
参考答案:(1)电子排布图:“略”;Cl;在氟化氢分子中存在氢键,分子间作用力大,破坏其作用力需要的温度较高,而氯化氢中不存在氢键,所以氟化氢的沸点高于氯化氢的沸点
(2)4;Ⅷ;铁;1s22s22p63s23p63d6
(3)Cl2+H2O==HCl+HClO
(4)CaF2;X射线衍射法;(8b+4c)/a NA
本题解析:
本题难度:困难
2、选择题 下列关于晶体与非晶体的说法中正确的是
[? ]
A.固体SiO2一定是晶体
B.晶体有自范性但排列杂乱无章
C.非晶体无自范性而且排列无序
D.非晶体一定比晶体的熔点高
参考答案:C
本题解析:
本题难度:简单
3、填空题 第三主族元素包括B、Al、Ga、In、Tl。
(1)在硼酸B(OH)3分子中,B原子与3个羟基相连,其晶体为层状结构。则分子中B原子杂化轨道的类型为?,同层分子间的主要作用为?。
(2)氯化铝在气态中常以二聚分子Al2Cl6形式存在,在Al2Cl6分子中存在的化学键的类型有 ?、?。
(3)砷化镓属于第三代半导体,它能直接将电能转化为光能,其晶胞结构如右图所示。
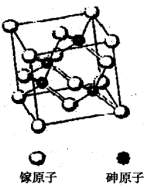
①Ga的基态原子的核外电子排布式为?。
②在砷化镓的晶胞结构中,镓原子的配位数为____?。
③在砷化镓的晶胞结构中,与同一砷原子相连的镓原子构成的空间构型为?。
参考答案:(1)SP2?氢键?(2)极性共价键、配位键
(3)①1S22S22P63P63d104s24p1?②4?③正四面体
本题解析:略
本题难度:一般
4、简答题 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于周期表的______区;溴的价电子排布式为______.
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是______.
(3)请根据表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是______.
| 氟 | 氯 | 溴 | 碘 | 铍
第一电离能
(kJ/mol)
1681
1251
1140
1008
900
|
(4)已知高碘酸有两种形式,化学式分别为H5IO6(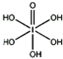 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6______HIO4.(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6______HIO4.(填“>”、“<”或“=”)
(5)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大这是由于溶液中发生下列反应I-+I2=I3-.与KI3类似的,还有CsICl2等.已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列______式发生.
A.CsICl2=CsCl+IClB.CsICl2=CsI+Cl2
(6)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为______,写出一个ClO2-的等电子体______.
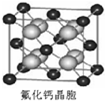
(7)已知CaF2晶体(见图)的密度为ρg?cm-3,NA为阿伏加德罗常数,最近相邻的两个Ca2+的核间距为acm,则CaF2的相对分子质量可以表示为______.
参考答案:(1)根据构造原理知,卤族元素最后填入的电子为p电子,所以卤族元素位于元素周期表的p区;溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,所以其价电子排布式为4s24p5,故答案为:p;4s24p5;
(2)HF分子之间存在氢键,使氢氟酸分子缔合,故答案为:氢键;
(3)卤族元素包含:F、Cl、Br、I、At元素,元素的第一电离能越小,元素失电子能力越强,得电子能力越弱,则越容易形成阳离子,根据表中数据知,卤族元素中第一电离能最小的是I元素,则碘元素易失电子生成简单阳离子,故答案为:I;
(4)H5IO6(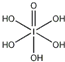 )中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,故答案为:<;
)中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,故答案为:<;
(5)离子晶体中离子电荷越多,半径越小离子键越强,离子晶体的晶格能越大,已知已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,所以发生的反应为CsICl2=CsCl+ICl,故答案为:A;
(6)ClO2-中心氯原子的价层电子对数n=2+7+1-2×22=4,属于sp3杂化;等电子体具有相同的电子数目和原子数目的微粒,所以与ClO2-互为等电子体的分子为Cl2O、OF2等,故答案为:sp3;Cl2O或OF2;
(7)该晶胞中含有钙离子个数=18×8+12×6=4,含有氟离子个数=8,近相邻的两个Ca2+的核间距为acm,则晶胞棱长=
本题解析:
本题难度:一般
5、填空题 [选修物质结构].铁是地球表面最丰富的金属之一,能形成多种配合物,铁系催化剂是工业生产中常用的催化剂。
(1)合成氨工业使用的催化剂是以铁为主体的多成分催化剂。
①NH3中N原子的杂化轨道类型是?。
②N与O同属第二周期,N的第一电离能比O大的原因是?。
③根据等电子体原理,写出一种NH4+是等电子体的微粒的化学式____________。
(2)二茂铁[(C5H5)2Fe]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右所示,其中氢原子的化学环境完全相同。

①Fe的基态电子排布式为____________。
②二茂铁中Fe2+与环戊二烯离子(C5H5-)之间的化学键类型是 _______________。
③1mol环戊二烯( )中含有σ键的数目为_________个。
)中含有σ键的数目为_________个。
(3)普鲁士蓝俗称铁蓝,结构如图所示,K+未画出),每隔一个立方体在立方体中心含有一个K+离子,普鲁士蓝中铁元素的化合价有+2和+3两种,其中Fe3+与Fe2+的个数比为:_____________。
参考答案:
⑴ ①sp3(1分)
②N原子失去的1个电子是相对稳定的半充满的2p能级上的电子,需要提供额外的能量,而O原子离去电子来自2p4构型,相对于2p3构型而言稳定性较差。(1分)
③CH4(1分)
⑵ ①[Ar]3d64s2或1s22s22p63s23p63d64s2(1分)? ②配位键(1分)? ③11NA(1分)
⑶ 1:1(2分)
本题解析:略
本题难度:一般