微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将溴水分别与酒精、己烯、苯和四氯化碳混合,充分振荡后静置,下列现象与所加试剂不相吻合的是( )
| ? | ?A | ?B | ?C | ?D
?与溴水混合的试剂
?酒精
?乙烯
?苯
?四氯化碳
?现象
?
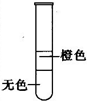
?

?

?
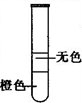
|
A.A
B.B
C.C
D.D
参考答案:A
本题解析:
本题难度:一般
2、选择题 为除去MgCl2溶液中的NaCl杂质,下列实验操作及其顺序正确的是
[? ]
①过滤 ②滴加过量的氢氧化钠溶液 ③滴加过量的硝酸银溶液 ④滴加适量的稀盐酸 A.②①④
B.①③④
C.①②④
D.②④③
参考答案:A
本题解析:
本题难度:一般
3、选择题 为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是
[? ]
不纯物
除杂试剂
分离方法
A.
CH4(C2H4)
高锰酸钾溶液
洗气
B.
苯甲酸(硫酸钾)
NaOH溶液
重结晶
C.
乙酸乙酯(乙酸)
饱和Na2CO3溶液
分液
D.
C2H5OH (H2O)
新制生石灰
过滤
参考答案:C
本题解析:
本题难度:一般
4、填空题 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于工业生产的漂白及消毒。
下图是过氧化氢法生产亚氯酸钠的工艺流程图:
相关物质的性质如下:
① ClO2沸点低易气化;浓度较高的ClO2气体易分解爆炸。
② NaClO2溶解度随温度升高而增大,适当条件下可结晶析出NaClO2・3H2O。

(1).在ClO2发生器中通入SO2的同时鼓入空气,其作用是________(填序号)。
A.将SO2氧化成SO3,增强酸性
B.稀释ClO2以防止爆炸
C.将NaClO3氧化成ClO2
(2)为确保H2O2充分参与反应,吸收塔内温度不宜较高,其原因是______________。
(3)160 g・L-1 NaOH溶液的物质的量浓度为______________,在实验室若要配制450mL该物质的量浓度NaOH溶液,应称取NaOH的质量为__________克。
(4)写出吸收塔内反应的化学方程式_____________________________________。
(5)从滤液中得到NaClO2・3H2O粗晶体的实验操作依次是____________(填序号)。
A.蒸馏? B.蒸发? C.灼烧? D.过滤? E.冷却结晶
要得到更纯的NaClO2・3H2O晶体必须进一步的操作是________(填操作名称)。
参考答案:(1)B(2分)
(2)H2O2受热易分解(2分)
(3)4mol/L、80克(2分)
(4)2ClO2 + H2O2 + 2NaOH = 2NaClO2 + 2H2O + O2↑(2分)
(5)B、E、D(2分) 重结晶(2分)
本题解析:(1)因为浓度较高的ClO2气体易分解爆炸,所以通入空气是稀释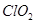 ,以防爆炸,B正确;
,以防爆炸,B正确;
(2)H2O2受热易分解;
(3)160/(23+16+1)=4,0.5*4*(23+16+1)=80,因为实验室没有450mL的容量瓶,需要用500mL的;
(4)根据流程信息可知,吸收塔内生成NaClO2,所以一定有ClO2→NaClO2,化合价降低,被还原;则H2O2必定被氧化,有氧气产生,反应方程式为2ClO2 + H2O2 + 2NaOH = 2NaClO2 + 2H2O + O2↑
(5)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶?体.所以操作顺序为BED,得到的粗晶体经过重结晶可得到纯度更高的晶体。
本题难度:困难
5、填空题 混合物分离的方法在生产、生活和科学实验中着广泛的应用。请指出下列做法中分别应用了哪些分离方法?
a.熬煮中药____________________;
b.分离豆浆和豆渣_____________________;
c.除去水中的沙子________________________;
d.用海水晒盐____________________;
e.海水淡化____________________;
f.从溴水中提取溴___________________。
参考答案:a.萃取;b.过滤;c.过滤;d.蒸发结晶;e.蒸馏;f.萃取
本题解析:
本题难度:一般