微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工业上利用反应:CO(g)+H2O(g) 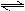 ?CO2(g)+H2(g);△H="Q" kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。
?CO2(g)+H2(g);△H="Q" kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。

若在一容积固定的密 闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
t/min
| CO(g)
| H2O(g)
| CO2(g)
| H2(g)
|
0
| 0.200
| 0.300
| 0
| 0
|
2
| 0.138
| 0.238
| 0.062
| 0.062
|
3
| c1
| c2
| c3
| c4
|
4
| c1
| c2
| c3
| c4
|
?
已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是_______.
A.单 位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q______0(填“>”、“=”或“<”).
(3)若在850℃时向反应容器中充入H2O(g),K值___ __(填“增大”、“减小”或“不变”).
__(填“增大”、“减小”或“不变”).
(4)达平衡时CO2的反应速率______,CO(g)的转化率为_______.
参考答案:(1)C(2)<(3)不变(4)0.04 mol/(L?min)?;? 60
本题解析:略
本题难度:一般
2、选择题 温度一定时, 于密闭容器中发生可逆反应: mA(气) + nB(气)  pC(气), 达到平衡后, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1 .9 倍, 则下列叙述中正确的是(?)
pC(气), 达到平衡后, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1 .9 倍, 则下列叙述中正确的是(?)
A.平衡向逆反应方向移动
B.C气体的体积分数增大
C.气体A的转化率升高
D.m + n > p
参考答案:A
本题解析:将混合气体的体积压缩到原来的 1/2的瞬间,C的浓度为原平衡时C的浓度的 2倍,但最终平衡时,C的浓度为原平衡时C的浓度的 1 .9 倍,这说明增大压强平衡向逆反应方向移动,则正反应是体积增大的可逆反应,所以答案选A。
点评:该题的关键是能够判断出压缩的瞬间和最终平衡时浓度的变化,从而得出平衡的移动方向。
本题难度:一般
3、选择题 一定条件下反应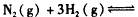
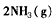 在10 L的密闭容器中进行,测得2 min内,N2的物质的量由20 mol减小到8 mol,则2 min内N2的反应速率为
在10 L的密闭容器中进行,测得2 min内,N2的物质的量由20 mol减小到8 mol,则2 min内N2的反应速率为
[? ]
A.1.2 mol/(L·min)
B.1 mol/(L·min)
C.0.6 mol/(L·min)
D.0.4 mol/(L·min)
参考答案:C
本题解析:
本题难度:简单
4、选择题
达到平衡后,下列说法中一定正确的是
A.平衡时,用A的浓度变化表示的正反应速率是用B的浓度变化表示的逆反应速率的a/b倍
B.保持容器内气体压强不变,再通入稀有气体,平衡不移动
C.保持容器体积不变,再通入一定量的C,建立新的平衡状态时,A的体积分数与原平衡时相同
D.保持容器体积不变,增加B的物质的量,建立新的平衡状态时,A的转化率升高
参考答案:AD
本题解析:本题考查化学平衡有关知识,属中等难度。平衡状态时,υ(A)/υ(B)=a/b,故A正确。压强不变,通入稀有气体,则平衡体系的压强减小,由于a、b、c三者数值不确定,故无法判断是否发生移动,B错误。保持容器体积不变,再通入一定量的C,建立新的平衡状态与原平衡互为等效平衡,故A的体积分数与原平衡时相同,C正确。增加B的用量,平衡必向正反应方向移动,A的转化率升高,D正确。
本题难度:一般
5、填空题 (12分)牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
 Ca5(PO4)3OH(固)
Ca5(PO4)3OH(固) 5Ca2++3PO43-+OH-
5Ca2++3PO43-+OH-
(1)进食后,细菌和酶作用于食物,产生有机酸,这时牙齿受腐蚀,其原因是?。(3分)
(2)已知Ca(PO4)3F(固)的溶解度比上面的矿化产物更小,质地更坚固。请用离子方程式表示:?(3分)
(3)当牙膏中配有氟化物添加剂后能防止龋牙的原因?。(3分)
(4)根据以上原理,请你提出一种其他促进矿化的办法:?。(3分)
参考答案:(1)生成的有机酸,中和OH-,使平衡向脱矿方向移动,加速牙齿腐蚀(2)5Ca2++3PO43-+F-=Ca5(PO4)3F↓(3)使用氟化物,增大了F-的浓度,促进了Ca(PO4)3F的生成。(4)加入Ca2+或PO43-。
本题解析:进食后,细菌和酶作用于食物,产生有机酸,使得Ca5(PO4)3OH固体减小,牙齿受到 腐蚀。使用氟化物,增大了F-的浓度,促进了Ca(PO4)3F的生成。促进矿化要使平衡向逆反应方向移动,可以增加生成物的浓度。
本题难度:一般