微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
(1)450℃时,往一个2L的密闭容器中充入2. 6mol H2和1mol N2, 反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
时间/min
| 5
| 10
| 15
| 20
| 25
| 30
|
c(NH3)/mol・L―1
| 0.08
| 0.14
| 0.18
| 0.20
| 0.20
| 0.20
|
①5 min内,消耗N2的平均反应速率为_______________,此条件下该反应的化学平衡常数K=_______________;反应达到平衡后,若往平衡体系中加入H2、N2和NH3各2mol,此时该反应的v(N2)正_______________v(N2)逆(填写“>”、“=”或“<”=)。
②下列各项能作为判断该反应达到化学平衡状态的依据是__________(填序号字母)
A.容器内N2、H2、NH3的浓度之比为1:3:2?
B.v(N2)正=3v(H2)逆 ?C.容器内压强保持不变?
D.混合气体的密度保持不变? E.容器内混合气体的平均分子量不变
③若改变某一条件,达新平衡时n(H2)="1.60mol" ,下列说法正确的是_____________。
A.平衡一定正向移动? B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度? D.可能是缩小了容器的体积
(2)450℃时,在另一密闭容器中进行上述合成氨的反应,各物质的起始浓度和平衡浓度如下表所示:
?
| N2
| H2
| NH3
|
起始浓度(mol/L)
| 0.2
| 0.3
| 0.2
|
平衡浓度(mol/L)
| a
| b
| c
|
请回答:
①各物质的平衡浓度可能是_______________.
A.c="0.5mol/L?" B.b="0.5mol/L?" C.c="0.4mol/L?" D.a=0.3mol/L
②a的取值范围是:_______________.
③请用数学表达式表示下列量之间的关系:
(I)a与b的关系:_______________。
(Ⅱ)a、b、c的关系:_______________。
(3) 根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水可发生下列反应:2N2(g)+6H2O(l)  4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“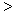 ”、 “
”、 “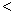 ”或“=”), △H=_____________。
”或“=”), △H=_____________。
(已知:H2的燃烧热为285.8 kJ/mol)
参考答案:(1)①0.008mol.L-1.min-1 ;? 0.1;?>? (每空1分)?②C E (2分)?③CD (2分)
(2)①B(1分) ② 0.1<a<0.3 (2分) ③( I )3a="b+0.3?" (2分)(Ⅱ)c2/(a×b3)="0.1" (2分)
(3)>? (1分)? +1530 kJ/mol? (2分)
本题解析:略
本题难度:一般
2、选择题 体积相同的密闭容器中均充入1 mol X和1mol Y,分别于300℃和500℃开始发生反应: X(g)+Y(g) 3Z(g),Z的含量(Z%)随时间t的变化如下图所示。
3Z(g),Z的含量(Z%)随时间t的变化如下图所示。

已知在t3时刻改变曲线b某一实验条件,下列判断正确的是
A.曲线a是500℃时的图像
B.从0到t1时刻,反应物X(g)的
C.t2时刻生成物Z的量
D.t3时刻改变的条件可能是降温
参考答案:D
本题解析:A、反应开始时b曲线的反应速率快,所以b的温度高,曲线b是500℃时的图像,错误;B、从0到t1时刻,b反应速率大于a,所以v(500 ?C)> v(300 ?C),错误;C、t2时刻生成物Z的量相同,所以△n(300 ?C)=△n(500 ?C),错误;D、从a到b,升高温度,Z的含量减小,说明升温,平衡逆向移动,正向是放热反应。t3时刻Z的含量增加,说明平衡正向移动,可能为降温或减小压强,正确,答案选 D。
本题难度:一般
3、选择题 某温度下,在一体积不变的密闭容器中充入1molN2O4气体,达到平衡后,再充入1mol N2O4气体,下列说法中错误的是
A.平衡向生成NO2的方向移动
B.新平衡相对旧平衡,N2O4的转化率增大
C.N2O4的浓度增大
D.混合气体的颜色加深
参考答案:B
本题解析:假设体积扩大一倍,可建立等效平衡。先体积不变,可以看出在上面的基础上,增大压强,平衡朝体积减小的方向移动,故两平衡进行比较,N2O4的转化率减小。B错误,CD正确。A、充入气体的瞬间,平衡朝生成NO2的方向移动。
本题难度:一般
4、填空题 (10分)H2A(酸):K1=4.310-6,K2=2.110-9。H2B(酸):K1=1.010-4,K2=6.310-8,在浓度相同的对应溶液中,用“>”、“<”或“=”填空。
(1)中和同浓度、同体积NaOH溶液时的用量:H2A溶液________H2B溶液;
(2)c (Na+):Na2A溶液________Na2B溶液;
(3)pH:H2A溶液________H2B溶液;
(4)酸分子的浓度:NaHA溶液________NaHB溶液;
(5) 酸根离子的浓度:NaHA溶液________NaHB溶液;
参考答案:(1)= (2)= (3)>(4)>(5)<
本题解析:略
本题难度:简单
5、填空题 (8分)(1)已知25℃时弱电解质电离平衡常数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。25℃时,将20mL 0.10 mol・L-1 CH3COOH溶液和20mL 0.10 mol・L-1HSCN溶液分别与20mL 0.10 mol・L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为:
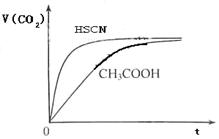
反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是?,
反应结束后所得两溶液中,c(CH3COO-)?c(SCN-)(填“>”、“<”或“=”)
(2)25℃时,将pH=1的H2SO4溶液a mL与pH=12的NaOH溶液b mL混合后,所得溶液的pH=3,则a:b=??;反应后,溶液中各离子浓度由大到小的顺序是??。
参考答案:(1)HSCN的酸性比CH3COOH强,其溶液中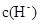 较大,故其溶液与NaHCO3溶液的反应速率快?<?(2)1 : 9;c(Na+)>c(SO
较大,故其溶液与NaHCO3溶液的反应速率快?<?(2)1 : 9;c(Na+)>c(SO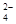 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
本题解析:(1)根据电离常数可知,HSCN的酸性比CH3COOH强,其溶液中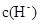 较大,故其溶液与NaHCO3溶液的反应速率快。酸越弱,相应的钠盐越容易水解。即醋酸钠溶液的碱性强于NaSCN溶液的碱性。所以c(CH3COO-)小于c(SCN-)。
较大,故其溶液与NaHCO3溶液的反应速率快。酸越弱,相应的钠盐越容易水解。即醋酸钠溶液的碱性强于NaSCN溶液的碱性。所以c(CH3COO-)小于c(SCN-)。
(2)根据题意硫酸过量,所以有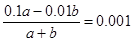 ,解得a:b="1" : 9。根据电荷守恒c(Na+)+ c(H+)=2c(SO
,解得a:b="1" : 9。根据电荷守恒c(Na+)+ c(H+)=2c(SO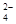 )+c(OH-)可知,溶液中各离子浓度由大到小的顺序是c(Na+)>c(SO
)+c(OH-)可知,溶液中各离子浓度由大到小的顺序是c(Na+)>c(SO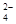 )>c(H+)>c(OH-)。
)>c(H+)>c(OH-)。
本题难度:一般