微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有四种短周期元素,它们的结构、性质等信息如下表所述。
元素
| 结构、性质等信息
|
A
| 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂
|
B
| B与A同周期,其最高价氧化物的水化物呈两性
|
C
| 元素的气态氢化物极易溶于水,可用作制冷剂
|
D
| 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂
|
?
请根据表中信息填写:
(1)A原子的核外电子排布式?。
(2)B元素在周期表中的位置?;
离子半径:B?A(填“大于”或“小于”)。
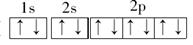
(3)C原子的电子排布图是?,其原子核外有?个未成对电子,能量最高的电子为?轨道上的电子,其轨道呈?形。
(4)D原子的电子排布式为?,D-的结构示意图是?。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为?,与D的氢化物的水化物反应的化学方程式为?。
参考答案:(1)1s22s22p63s1
(2)第3周期第ⅢA族 小于
(3)  ?3 p 纺锤
?3 p 纺锤
(4)1s22s22p63s23p5或[Ne]3s23p5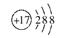
(5)NaOH+Al(OH)3=NaAlO2+2H2O? 3HCl+Al(OH)3=AlCl3+3H2O
本题解析:根据题中信息可推出:A为Na,B为Al,C为N,D为Cl。
(1)Na原子核外电子排布式为1s22s22p63s1。
(2)B为Al,其在元素周期表中的位置为第3周期第ⅢA族,Na+与Al3+核外电子排布相同,核电荷数Al3+大于Na+,故r(Al3+)<r(Na+)。
(3)C为N,其电子排布图为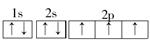 ,其中有3个未成对电子,能量最高的为p轨道上的电子,其轨道呈纺锤形。
,其中有3个未成对电子,能量最高的为p轨道上的电子,其轨道呈纺锤形。
(4)D为Cl,其核外电子排布式为1s22s22p63s23p5,简化电子排布式为 [Ne]3s23p5,Cl-的结构示意图为+17 288。
(5)本题考查Al(OH)3分别与NaOH、盐酸反应的方程式。
Al(OH)3+NaOH=NaAlO2+2H2O,Al(OH)3+3HCl=AlCl3+3H2O。
本题难度:一般
2、填空题 (10分)短周期元素A、B、C、D、E的原子序数依次增大,元素A是制备一种高效电池的重要材料,B原子的最外层电子数是内层电子数的2倍,C元素的气态氢化物与它的最高价氧化物能发生化合反应,元素D是地壳中含量最丰富的金属元素,E原子的最外层电子数是其电子层数的2倍。
(1)写出A作电极材料时的电极反应式: 。
(2)用电子式表示元素B与E形成化合物的过程: 。
(3)写出D的单质与氢氧化钠溶液反应的化学方程式:
。
(4)用D的单质在野外焊接钢轨的反应为: 。
(5)写出铜单质与C的最高价氧化物水化物的浓溶液反应的化学方程式:
。
参考答案:Li-e-=Li+ 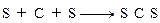 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+Fe2O3 Al2O3+2Fe Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Al2O3+2Fe Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
本题解析:略
本题难度:简单
3、填空题 (12分)U、V、X、Y、Z五种短周期元素,原子序数依次增大。U、V两元素最高正价与最低负价之和均为0;Y与U同主族;X、Z分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(用实际元素符号表示)________________;
(2)由这五种元素中的几种组成的化合物A、B、C、D有如下转化关系:

其中C是溶于水显酸性的气体;D是淡黄色固体。写出C与D反应的化学方程式:___________________;
①如果B为两性不溶物,则A的化学式为_________,A转化为B的离子方程式为:__?__________;
②如果B由四种元素组成且溶液显碱性,则B含有的化学键类型是_______,A所属物质类别为_ ___________(填选项序号)。a.酸? b.碱? c.盐? d.氧化物
参考答案:(1)Na>Al>C>O>H ?(2) 2Na2O2 + 2CO2 = 2Na2CO3 + O2
①Na[Al(OH)4];[Al(OH)4]-+CO2 ?= Al(OH)3↓+ HCO3-②离子键、共价键;c
本题解析:由“X、Z分别是地壳中含量最高的非金属元素和金属元素”知,X为氧元素,Z为铝元素,由“U、V两元素最高正价与最低负价之和均为0”,知两元素可能位于第ⅠA族或第ⅣA族,结合“U、V、X、Y、Z五种短周期元素,原子序数依次增大”和“Y与U同主族”知,U为氢元素,V为碳元素,Y为钠元素。(l)结合原子半径比较原则知,五种元素原子半径由大到小的顺序是Na>Al>C>O>H;(2)由这五种元素中的几种组成的化合物A、B、C、D有如下转化关系: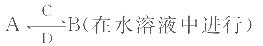 其中C是溶于水显酸性的气体;D是淡黄色固体。则C为CO2,D为Na2O2,二者反应的化学方程式为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;①B为两性不溶物,结合转化关系可知,A为四羟基合铝酸钠、B为氢氧化铝,四羟基合铝酸根与二氧化碳反应生成氢氧化铝,反应离子方程式为:[Al(OH)4]-+CO2 ?= Al(OH)3↓+ HCO3-;②B由四种元素组成,B溶液显碱性,结合转化关系可知,A为碳酸钠、B为碳酸氢钠,碳酸氢钠在化学键类型为离子键、共价键;碳酸钠属于盐。
其中C是溶于水显酸性的气体;D是淡黄色固体。则C为CO2,D为Na2O2,二者反应的化学方程式为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;①B为两性不溶物,结合转化关系可知,A为四羟基合铝酸钠、B为氢氧化铝,四羟基合铝酸根与二氧化碳反应生成氢氧化铝,反应离子方程式为:[Al(OH)4]-+CO2 ?= Al(OH)3↓+ HCO3-;②B由四种元素组成,B溶液显碱性,结合转化关系可知,A为碳酸钠、B为碳酸氢钠,碳酸氢钠在化学键类型为离子键、共价键;碳酸钠属于盐。
本题难度:一般
4、选择题 除去下列物质中的少量杂质(括号内为杂质),所选试剂正确的是
A.乙烷(乙烯)――通过溴水
B.Na2CO3(NaHCO3)――加盐酸
C.NO(NO2)――通人氧气
D.Cu(CuO)――加热
参考答案:A
本题解析:
本题难度:一般
5、选择题 在一定容积的容器中,加入a mol氙气和b mol氟气,在2635千帕和400℃下加热数小时后迅速冷却至室温(25℃),除剩余b/2 mol氟气外,还得到一种无色晶体,则所得无色晶体中,氙与氟的原子个数比为(氙气的化学式为Xe)
A.a∶b/2
B.a∶b
C.4a∶b
D.a∶2b
参考答案:B
本题解析:
本题难度:一般