微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铜锌原电池(如图)工作时,下列叙述正确的是( )
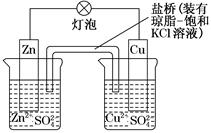
A.正极反应为:Zn―→Zn2++2e-
B.电池反应为:Zn+Cu2+=Zn2++Cu
C.在外电路中,电子从正极流向负极
D.盐桥中的K+移向ZnSO4溶液
参考答案:B
本题解析:在原电池中,活泼的金属材料作负极,相对不活泼的金属材料作正极,负极反应为:Zn―→Zn2++2e-,正极反应为:Cu2++2e-―→Cu,两个半反应相加,得出电池反应为:Zn+Cu2+=Zn2++Cu;D项,因Zn失电子,生成Zn2+,为使ZnSO4溶液中电荷保持电中性,盐桥中的Cl-移向ZnSO4溶液。
本题难度:一般
2、填空题 有一化学反应aA+bB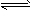 C,根据影响化学反应速率的因素可得v0=K{c(A)}m·{c(B)}n,其中K是与温度有关的常数。为测K、m、n的值,在298K时,将A、B溶液按不同浓度混合,得到下列实验数据
C,根据影响化学反应速率的因素可得v0=K{c(A)}m·{c(B)}n,其中K是与温度有关的常数。为测K、m、n的值,在298K时,将A、B溶液按不同浓度混合,得到下列实验数据
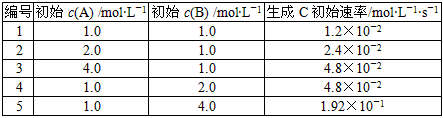
(1)根据上表可求得m=__________,n=__________,K=__________________。
(2)若a=m,当c(A)=c(B)=2mol·L-1时,求以B表示的初始反应速率。
____________________
参考答案:(1)1;2;1.2×10-2
(2)v(B)=1.92×10-1
本题解析:
本题难度:一般
3、计算题 丙酮和碘在酸性溶液中发生下列反应:CH3COCH3+I2→CH3COCH2I +H++I-。25℃ 时,该反应的速率由下列经验式决定:v=2.73×10-5c(CH3COCH3)c(H+) mol/(L·s)。25℃时,如果c(I2)、c(CH3COCH3)、
c(H+)的起始浓度依次是0.01mol/L、0.1mol/L、0.01mol/L,求:
(1)反应开始时的速率是多少?
(2)当溶液中的I2消耗一半时,反应速率比开始时慢还是快?
参考答案:(1)v0=2.73×10-8mol/(L·s)
(2)当I2消耗一半时,c(CH3COCH3)=0.1mol/L-1/2×0.01mol/L=0.095mol/L,
c(H+)=0.1mol/L+1/2×0.01mol/L=0.015mol/L,
此时的反应速率vt=2.73×10-5×0.095×0.015mol/(L·s)=3.89×10-8 mol/(L·s)
显然vt>v0,所以反应速率比开始时快。
本题解析:
本题难度:一般
4、选择题 X、Y、Z为三种气体,把amol X和bmol Y充入一密闭容器中,发生反应X+2Y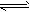 2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为
2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为
[? ]
A.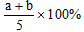
B.
C.
D.
参考答案:B
本题解析:
本题难度:一般
5、选择题 800℃时,某反应达到平衡,平衡常数K=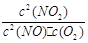 。恒容时,温度降低,NO浓度减小。下列说法正确的是( )
。恒容时,温度降低,NO浓度减小。下列说法正确的是( )
A.该反应是焓变为负值
B.恒温恒容下,通入Ar气以增大压强,则平衡右移
C.升高温度,逆反应速率减小
D.该反应化学方程式为2NO2(g)  2NO(g)+O2(g)
2NO(g)+O2(g)
参考答案:A
本题解析:根据平衡常数的表达式可知,方程式为2NO(g)+O2(g) 2NO2(g),D不正确。温度降低,NO浓度减小,说明平衡向正反应方向进行,即正反应是放热反应,S正确。B不正确,此时物质的浓度不变,平衡不移动。升高温度,反应速率都是增大的,C不正确。答案选A。
2NO2(g),D不正确。温度降低,NO浓度减小,说明平衡向正反应方向进行,即正反应是放热反应,S正确。B不正确,此时物质的浓度不变,平衡不移动。升高温度,反应速率都是增大的,C不正确。答案选A。
本题难度:一般