微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,下列溶液中一定能大量共存的离子组是( )
A.使pH试纸呈红色的溶液:Na+、[Al(OH)4]-、SO42-、Cl-
B.澄清透明溶液:Cr2O72-、SO42-、K+、NO3-
C.pH=0的溶液:Na+、C2O42-、Fe3+、NO2-
D.水电离产生的c(H+)=1×10-12mol?L-1的溶液:HCO3-、NH4+、Cl-、Ca2+
参考答案:A、使pH试纸呈红色的溶液含有H+,H+与[Al(OH)4]-生成Al(OH)3沉淀而不能大量共存,故A错误;
B、澄清透明溶液中Cr2O72-、SO42-、K+、NO3-不能发生离子反应,能大量共存,故B正确;
C、pH=0的溶液含有H+,在酸性溶液中C2O42-具有强氧化性,NO2-具有还原性,C2O42-与NO2-能发生氧化还原反应而不能大量共存,故C错误;
D、常温下,中性溶液中水电离的c(H+)=1×10-7mol?L-1,加入酸或碱抑制水的电离,所以水电离产生的c(H+)=1×10-12mol?L-1的溶液中含有H+或OH-,当含有H+时,H+与HCO3-生成水和二氧化碳而不能大量共存;当含有OH-时,HCO3-、OH-、Ca2+因生成水和碳酸钙沉淀而不能大量共存,NH4+与OH-生成一水合氨而不能大量共存,故D错误;
故选B.
本题解析:
本题难度:一般
2、填空题 有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO、CO中的一种或几种,取此溶液做下列实验:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气 体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:
体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:
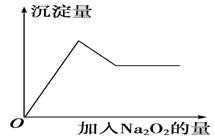
(1)溶液中一定含有的离子是______________  。
。
(2)溶液中肯定不含有的离子是_______________ _ 。
_ 。
(3)可能含有的离子是____________ 。
参考答案:(1) Mg2+、Al3+、SO42-。
(2)CO32-、H+、Cu2+、Fe3+
(3)Na+
本题解析:略
本题难度:简单
3、选择题 某溶液中含有大量Fe2+、Fe3+、Mg2+和NH4+,且c(H+)=0.1mol?L-1,则在该溶液中可以大量存在的阴离子是( )
A.SO42-
B.NO3-
C.SCN-
D.CO32-
参考答案:A.该组离子与SO42-均不发生反应,则离子能大量存在,故A正确;
B.因H+、Fe2+、NO3-发生氧化还原反应,则不能大量存在,故B错误;
C.因Fe3+、SCN-结合生成络离子,在额不能存在,故C错误;
D.因Fe3+、CO32-相互促进水解,Mg2+和CO32-结合生成沉淀,则不能共存,故D错误;
故选A.
本题解析:
本题难度:一般
4、选择题 列各组离子因发生氧化还原反应而不能大量共存的是
A.H+、Fe2+、MnO4-、SO42-
B.Ca2+、H+、SO42-、HCO3-
C.Na+、Cu2+、Cl-、OH-
D.Fe3+、K+、SCN-、Cl-
参考答案:A
本题解析:A、高锰酸具有强氧化性,能把亚铁离子氧化,不能大量共存,A正确;B、H+与HCO3-发生复分解反应生成CO2和水而不能大量共存,B不正确;C、Cu2+与OH-发生复分解反应生成氢氧化铜沉淀而不能大量共存,C不正确;D、Fe3+与SCN-发生络合反应生成Fe(SCN)3而不能大量共存,D不正确,答案选A。
本题难度:一般
5、选择题 实验室需配制一种仅含四种离子(不包括水电离出的离子)的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5 mol/L,下面四个选项中能达到此目的的是( )
A.Fe2+、Na+、NO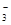 、Cl-
、Cl-
B.Mg2+、NH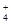 、SO
、SO 、NO
、NO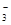
C.H+、K+、Cl-、CH3COO-
D.Fe3+、K+、AlO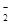 、SO
、SO