��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��8�֣���һ��������þ���Ͻ�Ͷ��100 mLһ��Ũ�ȵ������У��Ͻ���ȫ�ܽ⡣��������Һ�еμ�Ũ��Ϊ5 mol/L��NaOH��Һ�����ɵij����������NaOH��Һ�������ϵ��ͼ���������������λ��mL��������������λ��g����
 ?
?
��1������NaOH��Һ0--20mL�����з�Ӧ����ʽΪ��_______________________��160--180mL�����з�Ӧ����ʽΪ_______________________��
��2���Ͻ���Mg������Ϊ____________g������HCl�����ʵ���Ũ��Ϊ____________mol/L��
�ο��𰸣���1��HCl +NaOH�T�TNaCl+H2O ��Al��OH��3 +NaOH �T�TNaAlO2? +2H2O
��2��4.8?�� 8
�����������1������NaOH��Һ0--20mL��������Һ������������Ȼ����������������������������кͷ�Ӧ��HCl + NaOH�T�TNaCl+ H2O��
160--180mL�����г����������٣����������������������Ʒ����������ܽ⣺
Al��OH��3 + NaOH �T�TNaAlO2? +2 H2O
(2)Mg(OH)2��������11.6g,(��Al(OH)3���ڹ�����NaOH����NaAlO2.)
����Mg��Mg(OH)2��2HCl
24? 58? 2
m(Mg)? 11.6? n(HCl)
�������m(Mg)=4.8g
HCl��0.4mol
(2)��Ͻ�Ӧ��HCl��ʣ��
������0.02?5=0.1mol��NaOH.����HCl��0.1mol
3HCl��Al��Al(OH)3
3? 1? 78
n(HCl)? 7.8
���n(HCl)=0.3mol
һ������0.4mol +0.1mol +0.3mol =0.8molHCl
����c(HCl)=0.8/0.1=8mol/L
���������⿼������ļ��㣬ע���жϼ����NaOH��Һ��Ӧ�Ĺ��̣����������̵IJ���Ϊ������Ĺؼ���ͬʱ������ͼ��ķ���Ӧ��
�����Ѷȣ�һ��
2��ѡ���� ������Һ�е�C��Cl-��?��50mL1mol/L?AlCl3��Һ�е�C��Cl-��?��ȵ��ǣ�������
A��150mL3mol/LKCl��Һ
B��75mL2mol/LNH4Cl��Һ
C��150mL1mol/LNaCl��Һ
D��75mL1.5mol/LFeCl3��Һ
�ο��𰸣�50mL1mol/L?AlCl3��Һ��Cl-�����ʵ���Ũ��Ϊ3mol/L��
A��3mol/LKCl��Һ�������ӵ�Ũ��Ϊ3mol/L����A��ȷ��
B��2mol/LNH4Cl��Һ��Һ�������ӵ�Ũ��Ϊ2mol/L��1=2mol/L����B����
C��1mol/LNaCl��Һ�������ӵ�Ũ��Ϊ1mol/L����C����
D��1.5mol/LFeCl3��Һ������Cl-�����ʵ���Ũ��Ϊ1.5mol/L��3=4.5mol/L����D����
��ѡ��A��
���������
�����Ѷȣ�һ��
3��ѡ���� ��10.92 gп���Ͻ��ĩ���뺬0.4 mol H����ϡ�����ϡ����Ļ����Һ�У���ַ�Ӧ���ռ��õ��������������״���£�����Ϊ����������ȫ���ݳ���ϡ����Ļ�ԭ������NO��
A��2.4 L
B��3.6 L
C��4.8 L
D��6.0 L
�ο��𰸣�AB
���������п�Ļ�ԭ�Դ������Ļ�ԭ�ԣ�����п�ȷ�Ӧ������������Դ�������������ԣ����������ȷ�Ӧ����������ȫ��Ӧ������ֱ���п������Ӧ�����Կ�ʼ��Ӧ����NO����һ�ᷴӦ����H2��
����Ͻ�ȫ����п��п�����ʵ���=10.92g/65g/mol=0.168mol
������п��ȫ��Ӧ��ȫ����NO
3Zn+8HNO3=3Zn(NO3)2+2NO��+4H2O
3?8? 44.8
X? 0.4mol?Y
X=0.15mol<0.168mol��˵��п��������Y=2.24L
����Ͻ�ȫ���������������ʵ���=10.92g/56g/mol=0.195mol
����������ȫ��Ӧ��ȫ����NO
Fe(����)+4HNO3=Fe(NO3)3+NO��+2H2O
1? 4?22.4
X1? 0.4mol?Y1
X1=0.1mol<0.195mol��˵������������Y1=2.24L
3Fe(����)+8HNO3=3Fe(NO3)2+2NO��+4H2O
3? 8? 44.8
X2?0.4mol? Y2
X2=0.15mol<0.195mol˵��������
Y2=2.24L
������п��ȫ��Ӧ��ȫ����H2
Zn +2H+= Zn2+ + H2��
1? 2? 22.4
X3? 0.4mol? Y3
X3=0.1mol<0.168mol��˵��п������Y3=4.48L
����������ȫ��Ӧ��ȫ����H2
Fe +2H+= Fe2+ + H2��
1?2? 1
X4 ?0.4mol? Y4
X4=0.1mol<0.195mol��˵������������Y4=4.48L
������������֪��������Ӧ��2.24L��4.48L֮�䣬����ѡAB��
�����������ۺ���ǿ���Ѷȴ�ѧ����˼ά����������ߵ�Ҫ������������ѧ���������������ʹ���˼ά���������ѧ����Ӧ��������ѧ������������Ĺؼ������ú���ѧ�ϵļ�ֵ������һ���ۼ��ɡ�
�����Ѷȣ�һ��
4������� ��13�֣�����ijXY3����m g������Ħ������ΪM g��mol-1���������ӵ�������NA��ʾ����
��1������������ʵ���Ϊ?
��2������������ԭ������Ϊ?��
��3���������ڱ�״���µ� ���Ϊ?
���Ϊ?
��4�������� ����1Lˮ�У������Ƿ�Ӧ��
����1Lˮ�У������Ƿ�Ӧ�� ������Һ�����ʵ���������Ϊ?
������Һ�����ʵ���������Ϊ?
��5������������ˮ���γ�VL��Һ������Һ�����ʵ���Ũ��Ϊ?��
������Һ��ˮϡ����ԭ�����2������ȡ��50mLϡ�ͺ����Һ����ȡ����Һ�����ʵ���Ũ��Ϊ?
��6����״���£���ͬ�������һ������CH4������ԭ�ӵ����ʵ���Ϊ?
�ο��𰸣���13�֣���1��m/M?mol? (��ֵ�͵�λ����ȷ��1��)��2��4mNA/M?��2�֣�
��3��22.4m/M?L(2�֣���ֵ�͵�λ����1��)
��4��m/(m+1000)? (2�֣�Ҳ���Դ�100%����)
��5��m/MV mol��L -1?(2�֣���ֵ�͵�λ����1��) ?
?m/2MV mol��L -1(2�֣���ֵ�͵�λ����1��)
(6) 4m/M?mol? (2�֣���ֵ�͵�λ����1��)
�����������
�����Ѷȣ�һ��
5��ѡ���� ��NA��ʾ�����ӵ�������ֵ������������ȷ����
A��1molFeCl3���ˮ��Ӧ���ɽ������NA��Fe(OH)3����
B����״���£�1.12 L��HCHO������ԭ������0.2NA
C��1 L0.5mol��L-1Na2CO3��Һ�к��е�CO32����ĿΪ0.5NA
D��0.1 mol Na2O2��������ʱת�Ƶĵ�����Ŀ��0.2 NA
�ο��𰸣�B
���������A��FeCl3���ˮ������ȫ����Ӧ���ɽ��壬����B����״���£�1.12 L��HCHO������ԭ�����ǣ�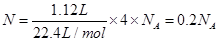 ����ȷ��C��CO32����ˮ�⣬����D��0.1 mol Na2O2��������ʱת�Ƶĵ�����Ŀ��0.1 NA������
����ȷ��C��CO32����ˮ�⣬����D��0.1 mol Na2O2��������ʱת�Ƶĵ�����Ŀ��0.1 NA������
�����Ѷȣ���