微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将铁粉加入到一定量的硝酸银、硝酸铜及硝酸锌的混合溶液中,待充分反应后过滤,在滤渣中加入稀盐酸,没有气体产生,则在滤液中(? )
A.只有硝酸锌和水
B.一定有硝酸锌和硝酸亚铁
C.一定没有硝酸银
D.一定没有硝酸铜
参考答案:B
本题解析:加入稀盐酸没有气体生成,则固体中没有Fe单质,所以一定有硝酸锌和硝酸亚铁,但却不能判断Ag和Cu是否都已经被完全置换出来了。
本题难度:简单
2、选择题 S2-和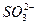 在酸性条件下可发生反应: S2-+
在酸性条件下可发生反应: S2-+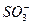 +H+――S↓+H2O(未配平),那么H+前的化学计量数应为(?)
+H+――S↓+H2O(未配平),那么H+前的化学计量数应为(?)
A.4
B.6
C.8
D.任意值
参考答案:B
本题解析:根据化合价升降法配平上述反应:2S2-+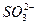 +6H+====3S↓+3H2O,故选B。
+6H+====3S↓+3H2O,故选B。
本题难度:简单
3、选择题 锌与很稀的硝酸反应生成硝酸锌、硝酸铵(NH4NO3)和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为
A.2 mol
B.1 mol
C.0.5 mol
D.0.25 mol
参考答案:D
本题解析:1mol硝酸锌生成,则转移2mol电子。硝酸在反应中氮元素的化合价从+5价降低到-3价,得到8个电子,所以被还原的硝酸是0.25mol,答案选D。
本题难度:简单
4、填空题 (1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
___________+___________ ___________+___________+___________+H2O
___________+___________+___________+H2O
(2)反应物中发生氧化反应的物质是___________,被还原的元素是___________。
(3)反应中1 mol氧化剂___________(填“得到”或“失去”) ___________mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
 ___________+
___________+ ___________
___________
参考答案:(1)FeSO4?HNO3?Fe(NO3)3?Fe2(SO4)3?N2O↑
(2)FeSO4?N
(3)得到?4
(4)24?FeSO4?30?HNO3
本题解析:由所给物质的特点可知,所组成的化学方程式应为氧化还原反应方程式,其中FeSO4作还原剂被氧化,HNO3作氧化剂,其中的氮元素由+5价降为+1价,被还原,1 mol HNO3应得4 mol电子。利用化合价升降法配平如下:


本题难度:简单
5、填空题 (8分)氰(CN)2?的结构简式为N≡C―C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素。(CN)2?和水反应可生成HCN和HCNO;(CN)2?的氧化性比Br2弱,比I2强。
(1)下列有关反应方程式不正确的是?(填选项标号)。
A.(CN)2?和NaOH溶液反应:(CN)2? + 2OH-= CN-+ CNO-+ H2O
B.MnO2和HCN反应:MnO2 + 4HCN  ?Mn(CN)2 + (CN)2?↑ + 2H2O
?Mn(CN)2 + (CN)2?↑ + 2H2O
C.向KCN溶液中加入碘水:I2 + 2KCN =" 2KI" + (CN)2
D.在NaBr和KCN混合溶液中通入少量Cl2:Cl2 + 2Br-= 2Cl-+ Br2
(2)HCN的电子式为?。
(3)处理含CN-(其中C为+2价)的工业废水常用ClO-氧化,生成的CNO-(其中C为+4价)元素,反应的离子方程式如下:aCN-+bClO-+2cOH-=dCNO-+eN2↑+fCO32-+bCl-+cH2O,上述化学方程式可能的配平系数有多组,请回答:
①方程式中e : f的值为?(填选项标号)。
A.1? B.1/2 ? C.2 ? D.不能确定
②若d=e=1,则b=?。
参考答案:(1)CD;?(2)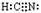 ;?(3)①B;? ②6
;?(3)①B;? ②6
本题解析:(1)根据(CN)2与水反应生成HCN和HCNO,可知(CN)2与NaOH溶液反应为(CN)2? + 2OH-= CN-+ CNO-+ H2O,A正确,根据氧化性Cl2>Br2>(CN)2>I2,可知MnO2和HCN能反应生成(CN)2?:MnO2 + 4HCN  ?Mn(CN)2+ (CN)2?↑ + 2H2O,B项正确,C、D项错误。
?Mn(CN)2+ (CN)2?↑ + 2H2O,B项正确,C、D项错误。
(2)HCN的电子式为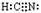 。
。
(3)根据原子守恒可知e:f=1:2。根据电荷守恒和原子守恒可知当d=e=1时,a=2,b=6,c=1,f=2。
点评:本题主要根据氧化性强弱、守恒法进行判断。
本题难度:一般