微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)沙里淘金是利用沙子与金子的______不同,用水流使沙子与金子分离开.
(2)粗盐提纯时,在除泥沙阶段中各步都用到的仪器是______.
(3)蒸馏操作分离两种液体时,液体的沸点最好相差20℃以上.蒸馏所用玻璃仪器有:酒精灯、______、牛角管、锥形瓶.
(4)泡药酒也是一种萃取,就是用酒精做萃取剂萃取(日常说成提取)固体物质中的相关成分.用萃取剂从碘水里萃取碘时选择萃取剂的主要原则是:①______;②______.
参考答案:(1)金的密度比较大,可用水洗法淘金,故答案为:密度;
(2)在除泥沙阶段中用到溶解和过滤操作,其中溶解用到烧杯、玻璃棒,过滤用到漏斗、烧杯、玻璃棒,则都用到玻璃棒,故答案为:玻璃棒;
(3)蒸馏操作需要铁架台、酒精灯、石棉网、温度计、冷凝管、牛角管、锥形瓶等仪器,则缺少蒸馏烧瓶、温度计、冷凝管,
故答案为:蒸馏烧瓶、温度计、冷凝管;
(4)萃取剂应与水不互不相溶、与被萃取的物质不反应,且最萃取的物质在萃取剂中的溶解度较大,
故答案为:此萃取剂与水互不相溶;碘在此萃取剂中的溶解度比在水中的溶解度.
本题解析:
本题难度:一般
2、选择题 下列属于分离、提纯固态有机物的操作的是?
A.蒸馏
B.分馏
C.重结晶
D.分液
参考答案:C
本题解析:略
本题难度:简单
3、选择题 下列说法正确的是
选项
| 实验
| 解释或结论
|
A
| 用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色
| 该溶液中一定含有Na+,
无K+
|
B
| 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧
| CO2、H2O与Na2O2反应是放热反应
|
C
| 向溴水中滴入植物油,振荡后,油层显无色
| 溴不溶于油脂
|
D
| 将硫酸酸化的H2O2滴入Fe(NO3)2溶液,溶液变黄色
| H2O2的氧化性比Fe3+强
参考答案:B
本题解析:A、因黄色光能遮挡紫色光,观察钾元素的焰色反应要通过蓝色钴玻璃,否则无法观察到钾元素的颜色,用洁净的Pt蘸取某溶液进行焰色反应,火焰呈黄色,不能说明不含钾元素,错误;B、CO2、H2O与Na2O2反应是放热反应,放出的热量达到脱脂棉的着火点,所以脱脂棉着火, B正确;C、植物油中含有碳碳双键,能和溴发生加成反应,导致油层显无色,错误;D、双氧水和硝酸都具有氧化性,混合溶液呈黄色,不能说明氧化剂是双氧水,错误。
本题难度:一般
4、填空题 海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。

完成下列填空:
(1)氯碱工业主要以食盐为原料。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列操作,正确的操作顺序是?。
①过滤;②加过量的NaOH溶液;③加适量的盐酸;④加过量的Na2CO3溶液;⑤加过量的BaCl2溶液
a.②⑤④①③? b.①④②⑤③? c? d.⑤②④①③
(2)在实验室中可以用萃取的方法提取溴,可选用的试剂是________________,所用主要仪器的名称是____________________。
(3)步骤Ⅰ中用硫酸酸化可提高Cl2利用率的原因是?。
(4)步骤II反应的离子方程式__________________________________________。
(5)海水提溴蒸馏过程中,温度应控制在80~90℃,温度过高或过低都不利于生产 ,请解释原因?。
(6)Mg(OH)2沉淀中混有Ca(OH)2,可选用__________溶液进行洗涤除去。如直接加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,这样可简化实验步骤,你_______(选填“同意”,“不同意”)该说法,理由是?。
参考答案:(1)AD
(2)CCl4(或苯);分液漏斗
(3)酸化可抑制Cl2 、Br2与水反应
(4)Br2+SO2+2H2O→4H++SO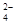 +2Br―(2分) +2Br―(2分)
(5)温度过高,大量水蒸气随水排除出,溴蒸气中水增加;温度过低,溴不能完全蒸出,吸收率低。(2分)
(6)MgCl2。不同意;MgO熔点很高,熔融时耗能高,增加生产成本。(2分)
本题解析:(1)除杂时为了把杂质除净除杂试剂需过量,除去粗盐中的Ca2+、Mg2+、SO42-分别选用Na2CO3溶液、NaOH溶液、?BaCl2溶液,前两中试剂可以用适量的盐酸除去,?BaCl2溶液只能放在加入Na2CO3溶液步骤前面,用其除去,注意加盐酸前过滤除去沉淀,故操作顺序为②⑤④①③?或⑤②④①③;
(2)萃取试剂不能与水互溶且被提取的物质在试剂中的溶解度要远大于在水中的溶解度,实验在分液漏斗中进行;
(3)Cl2 、Br2与水反应是可逆反应,酸化可抑制Cl2 、Br2与水反应;
(5)温度过高,大量水蒸气随水排除出,溴蒸气中水增加;温度过低,溴不能完全蒸出,吸收率低。
(6)选用MgCl2溶液,使Ca(OH)2转化为Mg(OH)2,同时洗去杂质;MgO熔点很高,熔融时耗能高,增加生产成本,故不用电解熔融MgO制金属镁。
本题难度:一般
5、选择题 下列实验与物质粒子大小无直接关系的是(? )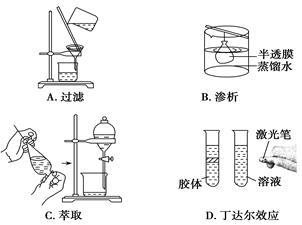
参考答案:C
本题解析:A为过滤,与粒子大小有关;B为渗析,胶体粒子不能透过而溶液中溶质粒子能透过;C为萃取,适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,与粒子大小无关;D为胶体的性质,丁达尔现象;
本题难度:一般
|