| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《阿伏伽德罗常数》高频试题特训(2017年最新版)(四)
(2)若反应在压强恒定、容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前<V后的是________;符合d前>d后和V前>V后的是________(填写反应的序号)。 (3)一定温度和压强下,混合气体对氢气的相对密度为21,则C2H4和C4H8的体积比为 ,混合气体中C2H4的质量分数为 。 参考答案:(1)B、C 本题解析:(1)在容积固定的容器内,四个反应的反应物和生成物中除硫单质外均为气体,所以反应B、C、D均符合d前=d后的关系式.反应B反应后气体物质的量减少,根据气态方程可知 本题难度:一般 3、选择题 设NA为阿伏伽德罗常数,下列叙述错误的是( ) 参考答案:A、12g镁与稀硝酸完全反应,电子转移是完全反应的金属镁失去的电子,12g镁物质的量为0.5mol,失去电子物质的量为0.5mol×2=1mol,故A正确; 本题解析: 本题难度:简单 4、选择题 决定气体体积的因素是( ) |
参考答案:C
本题解析:考查影响气体体积的因素。由于气体分子间的距离远大于气体分子直径大小,所以决定气体体积的因素是气体的物质的量多少和气体分子间的平均距离,答案选C。
本题难度:一般
5、选择题 有氢气和氧气的混合气体100mL,用电火花点火使其燃烧,再恢复到原温度和压强时,水为液态,气体体积减小为amL,则在原气体混合前,氢气的体积可能是
A.66.7-0.67a
B.66.7+0.67a
C.66.7-0.33a
D.66.7+0.33a
参考答案:A、D
本题解析:此题是求混合气体中某种气体所占体积大小的一种题型。氢气与氧气反应生成水,题中已明确生成的水为液态,则剩余的amL气体有两种可能,一个是未反应完的气体H2,一个是未反应完的气体O2。混合气体100mL,最后剩余气体amL,那么,消耗的体积就是(100-a)mL,根据阿伏加德罗定律,在化学反应方程</PGN0089B.TXT/PGN>中,系数比等于物质的量之比,也等于同温同压下气体各物质的体积比。
氢气与氧气正好完全反应时,体积比等于系数比是2∶1。所以氢
设氧气恰好反应,氢气有剩余时;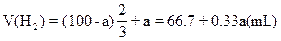
设氢气恰好反应,氧气有剩余时;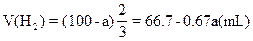
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《化学平衡常.. | |