| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《原电池原理》在线测试(2017年最新版)(二)
参考答案:D 本题解析:A.电极2通入的是氧气,是电源的正极,发生还原反应,A错误;B.电池工作时,阳离子Na+ 向正极移动,B错误;C.电极1是负极,则电流由电极2经外电路流向电极1,C错误;D.电极1是负极,失去电子,发生氧化反应,则发生的电极反应为:2NH3+6OH―-6e-=N2↑+6H2O,D正确,答案选D。 本题难度:一般 3、填空题 (14分)目前燃料电池中能量转化效率最高的是陶瓷电池,此类电池正面涂有黑色的稀有金属复合氧化物,作为正极,反面是一层较厚的绿色“金属陶瓷”,作为负极。在750℃实验温度下,空气中的氧分子吸附于黑色正极,氧原子会分别从涂层中“抢走”2个电子,变成氧离子,随后氧离子穿过陶瓷膜,与负极那一边的燃气反应,并释放出能量,氧不断“劫持”电子穿越薄膜,正负两极间便形成电压,产生电流。 参考答案:(1)CO、H2(2分) 本题解析:略 本题难度:一般 4、选择题 如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( ) |
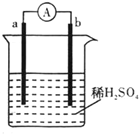
参考答案:A、碳棒上氢离子得电子生成氢气,所以有气体放出,故A正确.
B、根据“a的金属性比氢要强,b为碳棒”判断a为负极,b为正极,故B错误.
C、该装置形成了原电池,电子由负极沿导线流向正极,通过B知,电子从a极流到b极,故C正确.
D、a为负极,负极上失电子发生氧化反应,故D正确.
故选B.
本题解析:
本题难度:一般
5、选择题 研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进
行发电,在海水中电池总反应可表示为: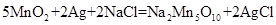 。
。
下列“水”电池在海水中放电时的有关说法正确的是:
A.正极反应式: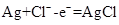
B.每生成2 mol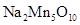 转移1 mol电子
转移1 mol电子
C.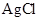 是还原产物
是还原产物
D.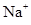 不断向“水”电池的正极移动
不断向“水”电池的正极移动
参考答案:D
本题解析:考查原电池的判断。在原电池中负极失去电子,发生氧化反应,电子经导线传递到正极,所以溶液中的阳离子向正极方向移动。正极得到电子,发生还原反应。根据总反应式可知,二氧化锰是氧化剂,作正极,每每生成1 mol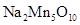 转移2 mol电子。银是还原剂,作负极,氧化产物是氯化银。所以正确的答案是D。
转移2 mol电子。银是还原剂,作负极,氧化产物是氯化银。所以正确的答案是D。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《氯及其化合.. | |