| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《原电池原理》在线测试(2017年最新版)(四)
参考答案:BC 本题解析:略 本题难度:一般 2、选择题 将纯锌片和纯铜片按图所示方式插入相同浓度的稀硫酸中,以下有关叙述中正确的是? 参考答案:A 本题解析:根据装置图可知,甲装置是原电池,化学能转化为电能。其中锌比铜活泼,做负极失去电子。铜是正极,溶液中的氢离子在正极得到电子生成氢气。乙装置是锌与稀硫酸直接发生的置换反应,但铜和稀硫酸不反应,所以选项A正确,其余选项均是错误的,答案选A。 本题难度:简单 3、选择题 如图所示,下列叙述中正确的是( ) |
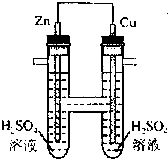
参考答案:由图可知,为Cu、Zn原电池,Zn为负极,
A.正极上发生还原反应,故A错误;
B.电子由负极(Zn)流向正极(Cu),故B错误;
C.负极Zn溶解,正极上析出氢气,故C错误;
D.正极上氢离子得电子生成氢气,故D正确;
故选D.
本题解析:
本题难度:一般
4、选择题 “便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e- = X + 2H+。下列说法中正确的是
A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2 + 4e- + 2H2O = 4OH-
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O
参考答案:D
本题解析:A.电池内部H+由正极向正极移动,错误;B.由于是酸性电解质溶液,另一极的电极反应式为:O2 + 4e- + 4H+= 2H2O,错误;C.乙醇在负极发生反应,电子经过外电路流向正极,错误;D正确;
考点:本题考查燃料电池为工作原理。
本题难度:一般
5、判断题 (10分)银器皿日久表面逐渐变黑色,这是由于生成硫化银,有人设计用原电池原理进行“抛
参考答案:
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《氯及其化合.. | |