微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 .可逆反应达到平衡的根本原因是(?)
A反应混合物中各组分的浓度相等? B.正逆反应都还在继续进行
C.正逆反应的速率均为零? D.正逆反应的速率相等
参考答案:D
本题解析:可逆反应达到平衡的根本原因是正逆反应的速率相等,且不为0,所以选项D正确,答案选D。
本题难度:简单
2、填空题 (8分)
一定温度下将3molA和1molB气体通入体积为2L的密闭恒容容器中,发生反应3A(g)+ B(g) xC(g)2min时反应平衡,剩余0.8molB,并测得C的浓度为0.4mol/L.
xC(g)2min时反应平衡,剩余0.8molB,并测得C的浓度为0.4mol/L.
回答问题
(1)从开始反应到达平衡,生成C的平均反应速率为________________
(2) x=________________
(3)若继续向原平衡混合物的容器中通入少量氦气,化学平衡___________(填字母)
A.向正反应方向移动
B. 向逆反应方向移动
C.不移动
(4)若向原平衡混合物的容器中再充入amolC,在原温度下达新的平衡,此时B的物质的量 n(B)=_______________mol
参考答案:每空2分0. 2? 4 ?C? 0.8+0.2a
本题解析:略
本题难度:一般
3、选择题 有A、B两个起始容积相等的恒温密闭容器,A保持恒压,B保持恒容.起始时向A、B中均通入2molSO2和1molO2后,在一定条件下反应达到平衡.则下列说法中不正确的是
A.达到平衡时,SO2的转化率:A<B
B.起始时的反应速率:A=B,反应完成时的平均速率:A<B
C.达到平衡后再充入等量氦气,A、B中平衡均不发生移动
D.若再向A中充入2molSO3,平衡时SO2的质量分数不变
参考答案:BCD
本题解析:2SO2+O2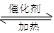 2SO3属于正反应气体系数减小的可逆反应,反应进行时气体的总物质的量减小,A容器恒压,容器内气体的压强不变,而B容器恒容,容器内气体的压强减小,故A相对于B来说,相当于加压
2SO3属于正反应气体系数减小的可逆反应,反应进行时气体的总物质的量减小,A容器恒压,容器内气体的压强不变,而B容器恒容,容器内气体的压强减小,故A相对于B来说,相当于加压
A:加压,平衡正向移动,SO2的转化率增大,故A>B,不正确
B:起始时两容器反应状态完全相同,反应速率相等,反应完成时,A容器内压强大,反应速率快,即A>B,不正确
C:达到平衡后再充入等量氦气,A容器相当于减压,平衡左移,而B容器内各物质的浓度不变,正逆反应速率仍旧相等,平衡不移动,不正确
D:在恒压情况下,若再向A中充入2molSO3,与原平衡等效,平衡时SO2的质量分数不变,正确
故答案为BCD
本题难度:一般
4、选择题 现向一密闭容器中充入1 mol N2和 3 mol H2,在一定条件下开始反应。下列有关说法中正确的是( )
A.达到化学平衡时,将生成2 mol NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应的速率都为零
参考答案:C
本题解析:该反应是可逆反应,所以不可能生成2mol氨气,A不正确;在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。所以C正确,D不正确。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此B不正确,答案选C。
点评:该题是高考中的常见考点,主要是考查学生对可逆反应平衡状态的熟悉了解程度,有利于培养学生的逻辑推理能力和抽象思维能力。该题的关键是理解并能熟练记住可逆反应的平衡状态特点,然后灵活运用即可。
本题难度:简单
5、选择题 一定条件下,在容积为1 L的密闭容器中发生可逆反应:Fe(s)+? H2O(g)=FeO(s)+H2(g)? ΔH>0。在1000℃时,H2O(g)的平衡转化率(α)与体系总压强(p)关系如图所示。
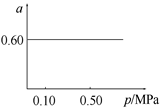
(1)当反应达到平衡后,再向容器中加入铁粉和水蒸气,则平衡常数K__________, (填“增大”、“减小”或“不变”);升高温度,则K__________。
(2)在1000℃时,若向上述容器中加入0.80 mol铁粉和1.00 mol水蒸气,达到平衡时,容器中c(H2)=______。
参考答案:(1)不变?增大?(2)0.6mol/L
本题解析:
(1)平衡常数只与温度有关。
(2)根据H2O(g)的平衡转化率是0.6,可以计算得到c(H2)=0.6mol/L
本题难度:一般