微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铜片和锌片用导线连接后插入稀硫酸中,电解质溶液的pH
[? ]
A.不变
B.先变小后变大
C.逐渐变小
D.逐渐变大
参考答案:D
本题解析:
本题难度:一般
2、选择题 一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料说法正确的是 (?)?
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O
C.通入空气的一极是负极,电极反应为:O2 + 4e- = 2O2-
D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O
参考答案:B
本题解析:在原电池中,阳离子移向正极,阴离子移向负极,故A错误;氧气发生得电子的还原反应,故通氧气的一极为原电池的正极,通丁烷的为原电池的负极,故C、D均错误;故选B。
本题难度:一般
3、填空题 (9分)设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,回答如下问题:
(1)以丁烷(C4H10)为汽油代表,这个电池放电时发生的化学反应 ;
(2)这个电池负极发生的反应是:C4H10 + 13O2― + 26e-=4CO2+5H2O,正极发生的反应是: ;固体电解质里O2-的移动方向是: ;向外电路释放的电子的电极是: ;
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是: ;
(4)汽油燃料电池最大的障碍是氧化反应不完全产生 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年,这正是新一代化学家的历史使命。
参考答案:

本题解析:略
本题难度:简单
4、选择题 有a、b、c、d四种金属,将a与b用导线连结起来浸入电解质溶液中,b不易腐蚀.将a、d分别投入等浓度的盐酸中,d比a反应剧烈.将Cu浸入b的盐溶液里,无明显变化.如果把Cu浸入c的盐溶液里,有c的单质析出.判断它们活动性由强到弱的顺序是
[? ]
A.d、c、a、b
B.d、a、b、c
C.d、b、a、c
D.b、a、d、c
参考答案:B
本题解析:
本题难度:一般
5、填空题 (16分)
Ⅰ、工业上用含有Cr2O72-和CrO42-的废水回收铬。其工艺流程如下:
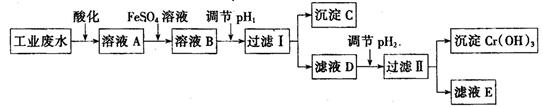
已知:①2 CrO42-(黄色)+2H+  Cr2O72-(橙色)+ H2O;
Cr2O72-(橙色)+ H2O;
②常温下,Ksp【Fe(OH)3】=1.0×10-38,Ksp【Cr(OH)3】=1.0×10-32;
③当离子浓度小于1.0×10-5mol・L-1时,认为沉淀完全。
(1)下列选项中能说明反应2 CrO42-(黄色)+2H+  Cr2O72-(橙色)+ H2O达平衡状态的是_______(填选项字母)。
Cr2O72-(橙色)+ H2O达平衡状态的是_______(填选项字母)。
A.Cr2O72-和CrO42-的浓度相同
B.2v(Cr2O72-)= v(CrO42-)
C.溶液的颜色不变
D.溶液的PH不变