|
|
|
���л�ѧ֪ʶ���ȫ��ԭ���ԭ������Ƶ����ǿ����ϰ��2017�����°棩(��)
2017-08-26 02:18:37
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� CO2��SO2��NOx �ǶԻ���Ӱ��ϴ�����壬���ƺ�����CO2��SO2��NOx �ǽ������ЧӦ����������⻯ѧ��������Ч;����
��1�����д�ʩ�У������ڽ��ʹ����е�CO2��SO2��NOx Ũ�ȵ���?������ĸ��
a�����ٻ�ʯȼ�ϵ�ʹ�ã���������Դ
b��ʹ�������䣬���ٷ��ﰺ�ŷ�
c���ಽ�л�˹�����������ר����˽�ҳ�
d������ҵ�����ü�Һ���պ����ŷ�
��2��Ϊ�˽�������β���Դ�������Ⱦ���йز������ü״������Ϊ��������ȼ�ϡ�д���úϳ���(CO��H2)�����״��Ļ�ѧ����ʽ?����֪�÷�Ӧ�ϳ�1 molҺ̬�״���������131.9 kJ�� 2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g)?��H =��594.1 kJ��mol��1����д��Һ̬�״�ȼ�����ɶ�����̼��ˮ�������Ȼ�ѧ����ʽ??��
��3��������������ͼ��ʾװ���õ绯ѧԭ����CO2��SO2ת��Ϊ��Ҫ����ԭ�ϡ�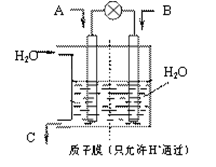
��AΪCO2��BΪH2��CΪCH3OH����ͨ��CO2��һ��Ϊ?������AΪSO2��BΪO2��CΪH2SO4�����ĵ缫��ӦʽΪ??��
��4�������о������������ת��ʱ��ijС����ĵ��������ݣ�17�桢1.01��105 Paʱ��
2NO2(g) 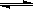 ?N2O4(g)?��H <0��ƽ�ⳣ�� K��13.3������������ܱ�������N2O4��NO2�Ļ������ﵽƽ��ʱ���� c (NO2) =" 0.0300" mol��L��1�� ?N2O4(g)?��H <0��ƽ�ⳣ�� K��13.3������������ܱ�������N2O4��NO2�Ļ������ﵽƽ��ʱ���� c (NO2) =" 0.0300" mol��L��1��
c (N2O4)��??��������λ��Ч���֣���
�ڸı�������ϵ��ij���������ﵽ�µ�ƽ���û�������� c (NO2) =" 0.04" mol��L��1�� c (N2O4) =" 0.007" mol��L��1����ı������Ϊ?��
�ο��𰸣���1��acd?��2�֣�
��2��CO��2 H2��CH3OH��2�֣�
2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g)? ��H =��1452 kJ��mol��1��3�֣�
��3������1�֣��� SO2��2H 2O��2e�� = SO42���� 4H+ ?��2�֣���
��4����0.012 mol��L��1?��2�֣��������¶ȣ�2�֣�
�����������1��ʹ�������䣬���ٷ��ﰺ�ŷţ������Ƴ������ƻ��ģ�b����ȷ���������ȷ�ģ���ѡacd��
��2��������֪�ķ�Ӧ����������֪������ʽΪCO��2H2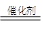 CH3OH����Ӧ��CO(g)��2H2(g) CH3OH����Ӧ��CO(g)��2H2(g)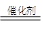 CH3OH(l)?��H =��131.9 kJ��mol��1���ͷ�Ӧ��2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g)?��H =��594.1 kJ��mol��1�����Ը��ݸ�˹���ɿ�֪�����ڣ��٣���2���õ� 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g)�����Է�Ӧ�ȡ�H =����594.1 kJ��mol��1��131.9 kJ��mol��1����2����1452 kJ��mol��1�� CH3OH(l)?��H =��131.9 kJ��mol��1���ͷ�Ӧ��2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g)?��H =��594.1 kJ��mol��1�����Ը��ݸ�˹���ɿ�֪�����ڣ��٣���2���õ� 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g)�����Է�Ӧ�ȡ�H =����594.1 kJ��mol��1��131.9 kJ��mol��1����2����1452 kJ��mol��1��
��3���ڷ�Ӧ��̼Ԫ�صĻ��ϼ۽��ͣ�����CO2�����������õ����ӣ����CO2������ͨ�롣SO2ʧȥ���ӣ��ڸ���ͨ�룬�缫��ӦʽΪSO2��2H 2O��2e�� = SO42���� 4H+ ��
��4���ٸ���ƽ�ⳣ������ʽ��֪��c (N2O4)��13.3��0.03002��0.012 mol��L��1��
�ڴ�ʱƽ�ⳣ����0.007��0.042��4.375����ƽ�ⳣ����С����������Ӧ�Ƿ��ȷ�Ӧ�����Ըı�������������¶ȣ�ƽ�����淴Ӧ�����ƶ���
�����Ѷȣ�һ��
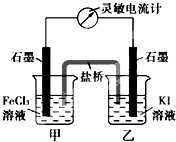
2��ѡ���� �����ʺϵ�����������Ӧ2Fe3++2I-=2Fe2++I2��Ƴ���ͼ��ʾ��ԭ��أ������жϲ���ȷ���ǣ�������
A�������ƶ���Ϊ����ڼ�������FeCl2���壬����ʯī�缫Ϊ����
B����Ӧ��ʼʱ������ʯī�缫��Fe3+����ԭ
C�������ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬
D����Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ
| 
�ο��𰸣�A��������Fe2+������ƽ�������ƶ�����Fe2+ʧȥ��������Fe3+����Ϊ������������ʯī��Ϊ��������A����
B�����ܷ�Ӧ����ʽ֪��Fe3+����ԭ��Fe2+��������ԭ��Ӧ����B��ȷ��
C����������Ϊ��ʱ��˵��û�е��ӷ���ת�ƣ���Ӧ�ﵽƽ�⣬��C��ȷ��
D��������I-ʧȥ���ӷŵ磬Ԫ�صĻ��ϼ����ߣ�����������Ӧ����D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ͼΪһԭ��صĽṹʾ��˼������˵���У�����ȷ���ǣ�������
A��ԭ��ع���ʱ���ܷ�ӦΪZn+Cu2+=Zn2++Cu���÷�Ӧһ��Ϊ���ȷ�Ӧ
B��ԭ��ع���ʱ��Zn�缫�������ӣ�����������Ӧ
C��ԭ��ع���ʱ��ͭ�缫�Ϸ���������Ӧ��CuSO4��Һ��ɫ����
D�������Cu�缫��ΪFe�缫��Zn�缫��Ȼ������
|

�ο��𰸣�A����ԭ��طŵ�ʱ���ϻ��õĽ���п��������������пʧ���ӷ���������Ӧ���ϲ����õĽ���ͭ��������������ͭ���ӵõ��ӷ�����ԭ��Ӧ�����Ե�ط�ӦʽΪ��Zn+Cu2+=Zn2++Cu���ҹ���ԭ��ص�����֮һ�ǣ���ѧ��Ӧ���������Է����е�������ԭ�ҷ��ȵķ�Ӧ���÷�Ӧ��һ�����ȷ�Ӧ����A��ȷ��
B��ԭ��ع���ʱ���ϻ��õĽ���п��������пʧȥ���ӷ���������Ӧ�����Ե��Ӵ�п����������B��ȷ��
C��ԭ��ع���ʱ���ϲ����õĽ���ͭ��������������ͭ���ӵõ��ӷ�����ԭ��Ӧ��������������ͭ������������
CuSO4��Һ��ɫ��dz����C����
D�������Cu�缫��ΪFe�缫��п�Ľ����Դ�����������Zn�缫��Ȼ����������D��ȷ��
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� ������������Դ���������й㷺��;������(Ni)�������缫���ŨNaOH��Һ�Ʊ���������(Na2FeO4)��װ����ͼ��ʾ������˵����ȷ����
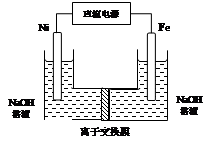
A�������������缫��ӦΪFe��2e����2OH��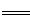 Fe(OH)2
Fe(OH)2
B�����һ��ʱ������缫������Һ��pH��С
C�������ӽ���ĤΪ�����ӽ���Ĥ����������������Һ�к���FeO42��
D��ÿ�Ƶ�1mol Na2FeO4�������Ͽ��Բ���67.2L����
�ο��𰸣�C
���������������Ni���������缫���ŨNaOH��Һ�Ʊ��������ƣ�Na2FeO4������ʧ�������ɸ������ƣ�������������������������������ʧ���������������ӣ��������Ӻ����������ӷ�Ӧ�������������������Ե缫��ӦʽΪFe-2e��+2OH���TFe(OH)2����A��ȷ�����缫�������ӷŵ�����������������Ũ�ȼ�С��������Һ��pH����B���������ӽ���ĤΪ�����ӽ���Ĥ���������������ƶ�������������Ҳ���Һ�к���FeO42������C�����¶Ⱥ�ѹǿδ֪���������������������������D����ѡA��
�����Ѷȣ���
5��ѡ���� X��Y��Z��M�������ֽ���Ԫ�أ�����X��Z�õ������ӷ���ϡ������ʱ��X�ܽ⣬Z�����������ų��������Y2+��Z2+�������Һʱ��Y��������ʹ�ö��Ե缫������֪M2+��������ǿ��Y2+���������ֽ����Ļ����ǿ������˳��Ϊ
[? ]
A��X>Z>Y>M
B��X>Y>Z>M
C��M>Z>X>Y
D��X>Z>M>Y
�ο��𰸣�A
���������
�����Ѷȣ�һ��



 Fe(OH)2
Fe(OH)2