微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述能证明次氯酸是一种弱酸的是
[? ]
A.次氯酸不稳定,易分解?
B.次氯酸是一种强氧化剂
C.次氯酸钙能与碳酸作用生成碳酸钙和次氯酸?
D.次氯酸能使染料和有机色质褪色
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
[? ]
A. 将 固体加入新制的氯水中,有无色气泡(
固体加入新制的氯水中,有无色气泡( )
)
B. 向 溶液中滴加新制氯水,再滴加
溶液中滴加新制氯水,再滴加 溶液,发现呈红色(
溶液,发现呈红色( )
)
C. 将 溶液滴加到新制氯水中,有白色沉淀产生(
溶液滴加到新制氯水中,有白色沉淀产生( )
)
D. 新制氯水使红色布条褪色( )
)
参考答案:D
本题解析:
本题难度:简单
3、填空题 二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图:
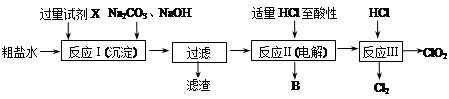
(1)粗食盐水中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,X是 ? (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42-,其原因是 ? 。(已知:Ksp(BaSO4)=1.1×10-10;Ksp(BaCO3)=5.1×10-9)
(2)上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成ClO2。电解时生成的气体B是 ? ;反应Ⅲ的化学方程式为 ? 。
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+―I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol・L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O32-=2I-+S4O62-)
① 准确量取10.00 mL ClO2溶液的玻璃仪器是 ? 。
② 滴定过程中,至少须平行测定两次的原因是 ? 。
③ 根据上述步骤可计算出原ClO2溶液的物质的量浓度为 mol・L-1(用含字母的代数式表示)。
参考答案:
(1)BaCl2? BaSO4和BaCO3的Ksp相差不大,当溶液中存在大量的CO32-离子时,BaSO4(s)会部分转化为BaCO3(s)
(2)H2? 2NaClO3+4HCl==2ClO2+2NaCl+2H2O
(3)酸式滴定管?减少实验误差?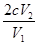
本题解析:(1)Na2CO3和NaOH分别除去 Ca2+、Mg2+,SO42-应用钡盐除去,考虑不能引入杂质,选用BaCl2溶液;由于BaSO4和BaCO3的Ksp相差不大,加入过量的Na2CO3,使得溶液中存在大量的CO32-离子,BaSO4(s)会部分转化为BaCO3(s)导致溶液中含有一定量的SO42-;(2)电解时氯元素化合价升高得到ClO2,另一极应是化合价降低的产物,故为氢气;(3)①精确的小数点后两位的溶液体积可以用滴定管或移液管;②滴定时为了减少实验误差,要做2~3次平行实验;③配平步骤2方程式,得出关系式2ClO2――5I2――10S2O32-
n(ClO2)=C V2×10-3÷5= 2C V2×10-4mol
c(ClO2)=2C V2×10-4÷V2×10-3×10=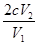 mol
mol
本题难度:困难
4、计算题 已知Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反 应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。
应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。
(1)写出Cl2在70℃的NaOH水溶液中符合上述条件的总反应方程式
(2)计算完全反应后生成物NaClO3的物质的量浓度
参考答案:
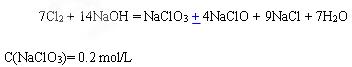
本题解析:略
本题难度:一般
5、选择题 关于卤素(用X表示)的下列叙述中正确的为( )
A.卤素单质与水反应的通式为X2+H2O= HX+HXO
B.HX都极易溶于水,它们的热稳定性随核电荷数增大而增强
C.卤素单质的颜色随相对分子质量增大的顺序不断加深
D.X-的还原性随卤素的核电荷数增大而增强,核电荷数小的卤素单质可将核电荷数大的卤素从它的盐溶液里置换出来
参考答案:C
本题解析:氟是最强的非金属元素,单质氟极易与水反应,即单质氟通入水中,只和水反应,所以A、D不正确。非金属性越强,相应氢化物的稳定性就越强,B不正确。答案是C。
本题难度:一般