|
���л�ѧ֪ʶ���ȫ���������ת������Ƶ����ǿ����ϰ��2017�����°棩(��)
2017-08-26 02:21:09
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���¸���Ӧ�У�����������������ڷ�Ӧ������������ǣ�?��
A������ȼ��
B��Ba��OH��2��8H2O��NH4Cl��Ӧ
C����Ƭ�����ᷴӦ
D����������ˮ��Ӧ
�ο��𰸣�B
�������������������������ڷ�Ӧ�������������˵���÷�Ӧ�����ȷ�Ӧ��ѡ��ACD���Ƿ��ȷ�Ӧ��B�����ȷ�Ӧ����ѡB��
�����������ǻ���������Ŀ��飬���������ǿ�����ض�ѧ������֪ʶ�Թ��̺�ѵ�����ѶȲ�����Ĺؼ��Ǽ�ס�����ķ��ȷ�Ӧ�����ȷ�Ӧ����һ�������ˮ���ᷴӦ������кͷ�Ӧ��һ��ȼ�գ���������Ϸ�Ӧ���û���Ӧ������������Ӧ��������Ƿ��ȷ�Ӧ��������ֽⷴӦ����κͼӦ��̼��������CO����ԭ���ķ�Ӧ�������ȷ�Ӧ��
�����Ѷȣ���
2��ѡ���� ����˵���������
A����֪298Kʱ��2SO2(g)��O2(g)  2SO3(g) ��H=��197kJ/ mol���Ը��Ȼ�ѧ����ʽ����Ϊ���ڸ������£����ܱ�������ͨ��2ĦSO2��1ĦO2���ﵽƽ��ʱ�ų�������197 kJ 2SO3(g) ��H=��197kJ/ mol���Ը��Ȼ�ѧ����ʽ����Ϊ���ڸ������£����ܱ�������ͨ��2ĦSO2��1ĦO2���ﵽƽ��ʱ�ų�������197 kJ
B��CO(g)��ȼ������283.0kJ/mol����2CO2(g)===2CO(g)��O2(g)��Ӧ�ġ�H��+��2��283.0��kJ/mol
C�����ȷ�Ӧ��ָ��Ӧ�������е����������������������е��������������ǿ���Ӧ�����Ƿ���Ҫ����
D�������з�Ӧ��HCl(aq) + NaOH(aq)="NaCl(aq)" + H2O(l)��H=��Q1kJ/mol
| 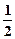 H2SO4(Ũ)+NaOH(aq)= H2SO4(Ũ)+NaOH(aq)= 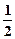 Na2SO4(aq)+H2O(l)?��H=��Q2kJ/mol Na2SO4(aq)+H2O(l)?��H=��Q2kJ/mol
������Ӧ������Һ�н��У���Q2>Q1
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
3������� ��8�֣���ͼ��ʾ�����Թܷ���ʢ��25��ʱ����ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ���5ml�������Թ��У��Իش��������⣺
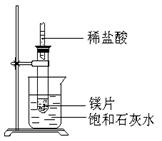
(1)ʵ���й۲쵽��������?
?��
(2)�����������ԭ��?
(3)д���йط�Ӧ�����ӷ�Ӧ����ʽ?
(4)�ɴ���֪��MgCl2��Һ��H2��������??������ڡ���С�ڡ����ڡ���þƬ�������������
�ο��𰸣���1����þƬ����������ݣ����٣��ձ����й�������������
��2��þ�����ᷴӦ�������������ų�������Ca(OH)2���ܽ�����¶ȵ����߶���С��
��3��Mg+2H+�TMg2++H2�� 2��?��4����
���������þ�ǻ��õĽ����������ᷴӦ�����Ȼ�þ�����������ڷ�Ӧ��������������������������������Ƿ��ȷ�Ӧ�����ڷ�Ӧ���ȣ�ʹ��Һ���¶����ߡ�����ΪCa(OH)2���ܽ�����¶ȵ����߶���С�����Ի������������ƾ��塣
�����Ѷȣ�һ��
4������� ?(������1)��1 L 1.0 mol/LNaOH��Һ����35.2 g CO2���壬��Һ��CO32-��HCO3-�����ʵ���֮��Ϊ1��3����Ӧ�Ļ�ѧ����ʽΪ_______________________________________��
�ο��𰸣�5NaOH + 4CO2=? 3NaHCO3?+? Na2CO3 + H2O
���������35.2 g CO2������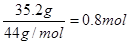 ������������1.0mol ������������1.0mol
�����ߵ����ʵ���֮����4�U5������Һ��CO32-��HCO3-�����ʵ���֮��Ϊ1��3
���Է���ʽΪ5NaOH + 4CO2=? 3NaHCO3?+? Na2CO3 + H2O��
�����Ѷȣ���
5������� ��16�֣�����β���dz��п�������Ҫ��Ⱦ��֮һ������Ҫ�к��ɷ���CO���������NOx���ȡ�
��1��NOx������ԭ��֮һ����������������ʱ����N2��O2��Ӧ���������仯ֵ����ͼ��ʾ��
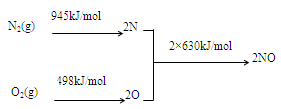
��N2(g)��O2(g) 2NO(g)?��H=����?�� 2NO(g)?��H=����?��
��2������β����CO��NOx����Ч������Ϊ�����������Ҫ���⡣ij�о�С����ʵ������ij���ʹ�����CO��NO��ת�������о������NOת��ΪN2��ת�������¶ȡ�CO������ı仯�������ͼһ��
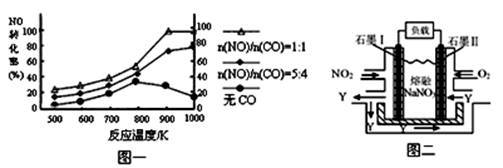
�� NO��CO���ʱ�����Ӧ�Ļ�ѧ����ʽΪ?��
�� 1000K��n(NO)/n(CO)=5:4ʱ��NO��ת����Ϊ75%����CO��ת����ԼΪ?��
�� ����n(NO)/n(CO)��ʵ�ʹ������Dz��ϱ仯�ģ���֤NOת���ʽϸߵĴ�ʩ�ǽ��¶ȴ�Լ������?K֮�䡣
��3������β����NOx����ͨ��ȼ�ϵ��ʵ��ת�����Ѿ������� NO2��O2������NaNO3�Ƴ���ȼ�ϵ�أ���ԭ����ͼ����
�� ͼ��ʯī��Ϊ��ص�?����
�� �ڸõ��ʹ�ù����У�ʯīI�缫�ϵIJ�����������Y����缫��ӦʽΪ?��
��4���״�Ҳ������ȼ�ϵ�ء���ҵ�ϲ��÷�ӦCO2(g)+3H2(g)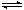 CH3OH(g)+H2O(g) ��H<0�ϳɼ״��� CH3OH(g)+H2O(g) ��H<0�ϳɼ״���
�� �ں����ܱշ�Ӧ���У�H2��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�
ϵ��ͼ����ʾ����A��B��C���㴦��Ӧƽ�ⳣ��(KA��KB��KC)��
��С��ϵΪ?��
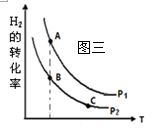
�� ij�����£���6molCO2��8molH2����2L�ܱ������з���
��Ӧ���ﵽƽ�����c(CO2)=2.0mol��L-1������¶��·�Ӧ��ƽ
�ⳣ��ֵΪ?��
�ο��𰸣�(16�֣�ÿ��2��)
��1�� +183 kJ��mol��1��2�֣�δд��λ��δд��+������1�֣�?
��2����2CO+2NO��N2 +2CO2��2�֣�δ��ƽ��1�֣��� ��93%����NOת������ý��Ϊ93.75%��������NO�����ֽ��Ӱ�죬ʵ��ֵ�������ֵ�в�࣬���Իش�93.75%�������ֵ�����֣� ��800��900
��3�� ��? NO2��NO3�� ��e�� ��N2O5
��4����KA��KB>KC?��1/2
�����������1����ͼ��֪���������ӵĹ��ۼ�������Ҫ����945kJ���������������ӵĹ��ۼ�������Ҫ����498kJ����������2N��2O��ϳ�2��NO���ӷų�1260kJ�����������ԡ�H=945+498-1260=+183kJ/mol��
��2����NO��CO���ʱ�����ɵ����Ͷ�����̼����ѧ����ʽΪ2CO+2NO��N2 +2CO2��
��1000K��n(NO)/n(CO)=5:4ʱ��NO��ת����Ϊ75%����NO�����ʵ�����5mol����CO�����ʵ�����4mol,����NO�����ʵ�����5mol��75%=3.75mol��������CO �����ʵ�����3.75mol������CO��ת����Ϊ3.75mol/4mol��100%=93.75%��
����ͼһ��֪����n(NO)/n(CO)Ϊ��ֵ��800-900KʱNO��ת���ʽϸߣ�����900K��������CO����ʱ��NO��ת�����������ߣ�����COʱNO��ת����ȴ���½������������˵��¶���800-900K֮�䣻
��3������������ԭ��Ӧ������ͨ�������ļ��ǵ�ص�������ʯīIͨ����Ƕ����������壬����������Ӧ������������NԪ�صĻ��ϼ���+4�ۣ�NԪ�ػ��ϼ�����ֻ�����ߵ�+5�ۣ�����������Y��N2O5���缫��ӦʽΪNO2��NO3�� ��e�� ��N2O5
��4����A��B����¶���ͬ������ƽ�ⳣ����ͬ��C���¶ȸ���B���¶����ߣ�������Ӧ������ƽ�������С���������ߵĴ�С��ϵ��KA��KB>KC��
��6molCO2��8molH2����2L�ܱ������з���CO2(g)+3H2(g)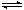 CH3OH(g)+H2O(g) ƽ�����c(CO2)=2.0mol��L-1�������Ķ�����̼��Ũ����1mol/L,����������Ũ����3mol/L�����ɵļ״���ˮ������Ũ�ȶ���1mol/L,������ƽ��Ũ����mol/L,����K=c(CH3OH)c(H2O)/c(CO2)c(H2)3=1/2 CH3OH(g)+H2O(g) ƽ�����c(CO2)=2.0mol��L-1�������Ķ�����̼��Ũ����1mol/L,����������Ũ����3mol/L�����ɵļ״���ˮ������Ũ�ȶ���1mol/L,������ƽ��Ũ����mol/L,����K=c(CH3OH)c(H2O)/c(CO2)c(H2)3=1/2
�����Ѷȣ�һ��
| 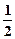 H2SO4(Ũ)+NaOH(aq)=
H2SO4(Ũ)+NaOH(aq)= 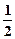 Na2SO4(aq)+H2O(l)?��H=��Q2kJ/mol
Na2SO4(aq)+H2O(l)?��H=��Q2kJ/mol