微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图所示,将铁棒和石墨棒插入饱和食盐水中。下列说法正确的是
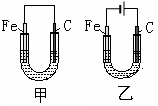
A.甲中铁被保护不会腐蚀
B.甲中正极反应式为4OH--4e- = 2H2O+O2?
C.乙中铁电极上发生氧化反应
D.乙中石墨电极附近滴几滴碘化钾淀粉溶液变蓝色
参考答案:D
本题解析:A.甲是原电池,铁作负极被腐蚀。碳作正极。错误。B. 甲中正极反应式为2H2O+4e-+O2=4OH-.错误。C.乙装置是电解池。Fe作阴极,阴极上发生还原反应。错误。D.乙中石墨电极为阳极。2Cl-―2e-=Cl2↑.Cl2+2I-=2Cl-+I2. I2遇淀粉溶液变蓝色。正确。
本题难度:一般
2、选择题 某原电池总反应为:Cu+2Fe3+?Cu2++2Fe2+,下列能实现该反应的原电池是(?)
?
| A
| B
| C
| D
|
电极材料
| Cu、Zn
| Cu、Ag
| ? Cu、C
| Fe、Zn
|
?电解液
| FeCl3
| Fe2(SO4)3
| Fe(NO3)2
| CuSO4
参考答案:B
本题解析:略
本题难度:一般
3、填空题 钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图所示:
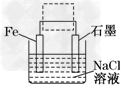
(1)写出石墨电极的电极反应式_____________________.
(2)将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改,并用箭头标出导线中电子流动的方向.
(3)写出修改后石墨电极的电极反应式_________________________________________.
参考答案:(1)2H2O+O2+4e-===4OH-(2)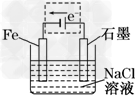 (3)2Cl--2e-===Cl2↑ (3)2Cl--2e-===Cl2↑
本题解析:
本题难度:一般
4、选择题 某化学兴趣研究小组设想将反应Zn+Br2=ZnBr2组成原电池。现在有下列四个电极反应:①Br2+2e-→2Br-;②2Br-→Br2+2e-;③Zn→Zn2++2e-;④Zn2++2e-→Zn,负极和正极的反应式分别为(?)
A.②③
B.②①
C.③①
D.④①
参考答案:C
本题解析:依据原电池的原理可知,负极是失电子的一极,且为电池总反应式中的反应物,故应为③Zn→Zn2++2e-;正极是得电子的一极,且也为电池总反应式中的反应物,故应为①Br2+2e-→2Br-。
本题难度:简单
5、简答题 (1)材料通常可分为金属材料、无机非金属材料、高分子合成材料等.玻璃、陶瓷、水泥属于______;三大合成材料是指:塑料、合成纤维和______.
(2)钢铁在潮湿的空气中更容易被腐蚀,主要原因是其中的铁和碳构成许多微小的______.
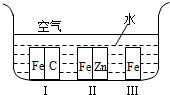
(3)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)______.
(4)下列关于铁制品保护措施的说法中不正确的有______(填序号,多选).
①在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
②相同条件下,马口铁(表层镀锡)与白铁(表层镀锌)相比,马口铁更为耐用
③在海轮的外壳上常焊有锌块,不必定期更新
④将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理.
参考答案:(1)玻璃、陶瓷、水泥的主要成分是硅酸盐类,属于无机非金属材料,塑料、合成纤维和合成橡胶是三大合成材料,故答案为:无机非金属材料;合成橡胶;
(2)钢铁在潮湿的空气中因为形成原电池装置原理,金属铁为负极材料,更易被腐蚀,故答案为:原电池;
(3)在各种腐蚀中,原电池的负极金属的腐蚀速率>化学腐蚀速率>原电池的正极金属腐蚀速率,故答案为:Ⅰ>Ⅲ>Ⅱ;
(4))①自行车钢圈上镀上一层金属铬,金属铬比金属铁活泼,金属铁可以充当原电池的正极,被保护,摩擦部位加上机油或黄油,可以隔绝空气,能防止金属铁被腐蚀,故①正确;
②马口铁(表层镀锡)中,金属活泼性是铁强于锡,金属铁做负极,白铁(表层镀锌)中,金属的活泼性是锌强于铁,金属锌为负极,负极金属易被腐蚀,正极金属被保护,马口铁更不耐用,故②错误;
③海轮的外壳上常焊有锌块做原电池的负极,更易被腐蚀,会有损耗,要定时补充,故③错误;
④将一些刀具进行烤蓝处理可以将金属隔绝空气,防止生锈,故④正确.
故答案为:②③.
本题解析:
本题难度:一般
|