微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室用下图所示装置来制取乙酸乙酯,回答下列问题:

(1)请写出本实验中发生的主要反应方程式?。
(2)配置混合溶液时,加入试剂的正确顺序是?(填“A”或“B”)。
A.先加乙醇,再慢慢注入浓硫酸和乙酸? B.先加浓硫酸,再慢慢注入乙醇和乙酸
(3)浓硫酸的作用是?。
(4)饱和Na2CO3溶液的作用是?。
(5)实验完成后,右边试管液面上有透明的不溶于水的油状液体生成。若要分离10mL该液体混合物需要用到的主要玻璃仪器是?,这种分离方法叫做?。
2、选择题 下图是某烃的含氧衍生物的比例模型。该有机物是

A.C2H5OH
B.C6H5OH
C.CH3CHO
D.CH3COOH
3、选择题 关于苯乙烯(?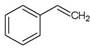 )的下列叙述,正确的是
)的下列叙述,正确的是
A.苯乙烯不可能发生加成反应
B.苯乙烯不可能使酸性高锰酸钾溶液褪色
C.苯乙烯不可能使溴的四氯化碳溶液褪色
D.苯乙烯可通过加聚反应生成高分子化合物
4、选择题 下列化合物中,显酸性的物质是(?)
A.CH2=CH―CH2OH
B.CH3COOH
C.CH2=CH―COOC2H5
D.CH3―CH―COOH
5、填空题 硫酸工业生产应考虑综合经济效益问题。
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在____的郊区。(填选项的序号) A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1 t 98%的硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应SO2(g)+1/2O2(g)=SO3(g);△H= -98.3kJ/mol-1放出的热量能在生产过程中得到充分利用,则每生产l t 98%的硫酸只需外界提供(或可向外 界输出)________千焦能量。
(3) CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3,和SO2,该反应的化学方程式为
______________________。
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4 (由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)。

已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因
___________________