��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣�ijͬѧ��̽��ʳ�������ӵ�Ĵ�����ʽ��ʵ���ҿ��ṩ����ҩƷ�����ۡ�ʳ�Ρ�H2O2��NaI��HCl��
��1����ͬѧҪѡ���ļ���ҩƷ���������ʵ��?��
��2��д����Ӧ�����ӷ���ʽ������˫��������ʾ����ת��?��
��3���ڸ÷�Ӧ�У���������?��?��ԭ����?��?
��4���ܹ��۲쵽����������Ϊ?��
��������ͻ�ԭ��������ʵ���֮��Ϊ?��
�ο��𰸣���1�����ۡ�ʳ�Ρ�NaI��HCl?��
��2��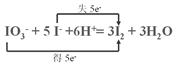
��3����������IO3-��?��ԭ����I-
��4����������Ϊ��������Һ������?���ʵ���֮��Ϊ 5 ��1
�����������
�����Ѷȣ�һ��
2��ѡ���� ����ĥ��������ƿ��ŵ��Լ��У�?��
A���ռ���Һ
B��Ũ����
C�������
D����������Һ
�ο��𰸣�B
����������Լ��ı���Ҫ��ҩƷ�����ʡ��ռ���Һ����ĥ��������ƿĥ�ڴ���SiO2��Ӧ����Na2SiO3��Na2SiO3������ԣ��ܽ�ƿ����ƿ�����һ��Ũ������лӷ��ԡ�ǿ�����ԣ����Ӧ�ܷⱣ����ĥ��������ƿ�С�������ܸ�ʴ��������Ӧ����ʽΪ��SiO2+4HF�T�TSiF4��+2H2O����������Һ�Լ��ԣ�Ҳ������ĥ��������ƿ��š�
�����Ѷȣ���
3��ѡ���� M(NO3)2���ȷֽ�Ļ�ѧ��Ӧ����ʽΪ��2 M(NO3)2 ="=" 2MO+4NO2��+O2��������29.6g M(NO3)2ʹ����ȫ�ֽ⣬�ڱ�״�����ռ�11.2L�����壬��ôM��Ħ�������ǡ�
A��65 g��mol-1
B��64g��mol-1
C��40 g��mol-1
D��24 g��mol-1
�ο��𰸣�D
����������ɷ���ʽ2 M(NO3)2 ="=" 2MO+4NO2��+O2����֪��2mol M(NO3)2 ��ȫ�ֽ�����5mol���壬�����29.6g M(NO3)2ʹ����ȫ�ֽ⣬�ڱ�״�����ռ�11.2L�����壬���Կɵ�M��Ħ��������24 g��mol-1
�����Ѷȣ�һ��
4������� ���ǵ����ϼ�Ϊ�ḻ��Ԫ�ء�
(1)Li3N�����е���N3-���ڣ���̬N3-�ĵ����Ų�ʽΪ?��
(2)N��N�ļ���Ϊ942 kJ��mol-1��N��N�����ļ���Ϊ247 kJ��mol-1������˵��N2�е�?����?���ȶ�������ҡ��С���
(3)(CH3)3NH+��AlCl4-���γ�����Һ�塣����Һ��������������ɣ��۵����100 �棬��ӷ���һ����л��ܼ�?�����С������������?������ţ���
a.��ȼ��? b.����ɫ���ܼ�? c.���ϲ���? d.���Ȳ���
(4)X+�����е������ó���K��L��M�������Ӳ㣬����N3-�γɵľ���ṹ��ͼ��ʾ��X��Ԫ�ط�����?����ͬһ��N3-������X+��?����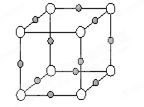
�ο��𰸣���1��1s2s22p6?��2����? ��?��3��С? b?��4��Cu? 6
�����������1�����ݹ���ԭ����֪����̬N3-�ĵ����Ų�ʽΪ1s2s22p6 ��
��2����������1���ļ���2�����γɵģ����ݼ��ܿ�֪���м����ܴ��ڦļ����ܣ���˦м��Ȧļ��ȶ���
��3�������۵��֪�����ӷ��Ա�һ���ܼ���Ҫ�ͣ������Ҫ��;�ǡ���ɫ���ܼ�����ѡb��
��4������X�Ľṹ��֪��XӦ����ͭ�����ݾ����ṹ��֪����ͬһ��N3-������X+��6���������¡����ҡ�ǰ��
�����Ѷȣ�һ��
5��ѡ���� ��(NH4)2CO3���ȵ�ȫ��ת��Ϊ�����������ͨ���������ƣ�������������x g����ͨ��Ũ���ᣬҺ����������y g������ͨ��Ũ���ᣬҺ����������z g����ͨ���������ƣ�������������w g����x��y��z��w�ɴ�С������˳����
A��z>y>x>w
B��w>z>y>x
C��y>z>w>x
D��x>y>z>w
�ο��𰸣�A
���������
���⻯ѧ��Ӧ:(NH4)2CO3=2NH3��H2O��CO2
2Na2O2��2H2O=4NaOH��O2
2Na2O2��2CO2=2Na2CO3��O2
2NH3��H2SO4=(NH4)2SO4
��ȡ1mol(NH4)2CO3,�ֽ����2molNH3��1molH2O��1molCO2
2Na2O2��2H2O=4NaOH��O2? ��m
1mol? 2g
2Na2O2��2CO2=2Na2CO3��O2?��m
1mol? 28g
��������ͨ���������ƣ�������������x g��
X=2g+28g=30g
2NH3��H2SO4=(NH4)2SO4?��m
2mol? 34g
��ͨ��Ũ���ᣬҺ����������y g
Y=34g
����ͨ��Ũ���ᣬҺ����������z=2mol��17g/mol+1mol��18g��mol-1=52 g��
��ͨ���������ƣ�������������w="28" g��
ѡA.
�����Ѷȣ���