微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
参考答案:B
本题解析:略
本题难度:一般
2、填空题 (13分)(1)配平氧化还原反应方程式:平衡时
__ C2O42-+__MnO4-+__H+= ?__CO2+__Mn2
?__CO2+__Mn2 ++__H2O
++__H2O
(2)称取6.0 g含H2C2O4・2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶液。量取两份此溶液各25mL,分别置于两个锥形瓶中。
(附相对原子质量:H--1? C--12? S--28? O--16? K--39 )?
①第一份溶液中加入酚酞试液,滴加0.25mol/L NaOH溶液至20mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为?mol。
②第二份溶液中滴加 0.10mol/L 的酸性高锰酸钾溶液至 16mL 时反应完全,此时溶液颜色由?变为?。该溶液中还原剂的物质的量为?mol。
③原试样中H2C2O4・2H2O的质量分数为?。
参考答案:(1)5? 2? 16? 10? 2? 8 (3分)
2? 16? 10? 2? 8 (3分)
(2)① 0.005(2分) ②无色;紫红色;(4分) 0.004(2分)③21%(2分
0.005(2分) ②无色;紫红色;(4分) 0.004(2分)③21%(2分 )
)
本题解析:(1)先标出变价元素的化合价,再根据得失电子守恒和原子守恒就可以配平;(2)①被中和的H+的物质的量就是消耗的NaOH的物质的量:0.25mol/L*20mL="0.005" mol ②酸性高锰酸钾溶液可以作为反应物也同时充当了指示剂,当恰好完全反应时溶液有无色变为紫红色;
5C2O42-~2MnO4-
n?0.10mol/L*16mL?所以n= 0.004,即该溶液中还原剂的物质的量为0.004 mol。原试样中H2C2O4・2H2O的质量分数为21%。
本题难度:一般
3、选择题 氰化物有剧毒,我国工业废水中氰化物(CN-)的最高允许排放浓度为0.5 mg/L;对废水中CN-的处理方法是:在碱性条件下,用Cl2将废水的中CN-转化成N2和CO2等,使废水得到净化。发生的反应为:2CN-+ 8OH-+ 5Cl2 = 2CO2 ↑+ N2 ↑+10 Cl-+ 4H2O ;下列有关说法正确的是(? )
A.上述反应中氧化产物只有N2
B.经测定,NaCN的水溶液呈碱性,说明CN―能促进水的电离
C.若上述反应生成0.4 mol CO2,则溶液中阴离子增加的物质的量为2 mol
D.现取1 L含CN-1.04mg/L的废水,至少需用4.0×10-5mol Cl2处理后才符合排放标准
参考答案:B
本题解析:CN-中碳元素的化合价是+2价,在反应中失去2个电子,生成CO2,所以CO2也是氧化产物,选项A不正确;NaCN的水溶液呈碱性,说明HCN一定是弱酸,则CN―能促进水的电离,发生水解使溶液显碱性,选项B正确;根据方程式可知,反应前后阴离子的个数是不变的,所以选项C不正确;1 L含CN-1.04mg/L的废水,要达到排放标准,则反应中就必须消耗0.54mgCN-,则根据方程式可知,需要氯气的物质的量是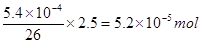 ,所以选项D也是不正确的,答案选B。
,所以选项D也是不正确的,答案选B。
本题难度:一般
4、选择题 在碱性条件下,可以用碘酸盐制备高碘酸盐:NaIO3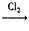 Na2H3IO6。下列有关该反应的说法中正确的是
Na2H3IO6。下列有关该反应的说法中正确的是
[? ]
A.该反应中H2O是反应物之一
B.NaIO3中I化合价为+5,而Cl2中Cl化合价为0,故NaIO3是氧化剂,Cl2是还原剂
C.上述反应中被氧化的元素原子个数与被还原的原子个数之比为2:1
D.反应中生成13.6 g Na2H3IO6,转移电子的物质的量为0.1 mol
参考答案:D
本题解析:
本题难度:简单
5、选择题 某炼金厂的废水因连降暴雨而溢出,导致河水严重污染,炼金废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸.下列说法不正确的是 ( ?)
A.CN-可以和稀硫酸反应生成HCN
B.CN-可被Cl2氧化成(CN)2
C.在水溶液中(CN)2不能将F-氧化
D.HCN的电子式为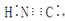
参考答案:D
本题解析:HCN为弱酸,则根据较强酸制备较弱酸的原理可知,选项A正确;CN-还原性介于I-与Br-之间,所以能被氯气氧化,B正确;(CN)2的氧化性弱于单质氟的,因此在水溶液中(CN)2不能将F-氧化,C正确;D不正确,电子式应该是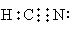 ,答案选D。
,答案选D。
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:简单