微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.2mol 溶液与lmol
溶液与lmol 溶液混合后,
溶液混合后, 2mol
2mol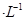
B.120gNaC1溶液中溶有20gNaCl,该温度下NaC1的溶解度为20g
C.22.4LHCl气体溶于水制成1L溶液,该溶液的物质的量浓度为lmol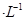
D.把5g胆矾(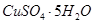 )溶于45g水中,所得溶液溶质的质量分数为10%
)溶于45g水中,所得溶液溶质的质量分数为10%
参考答案:A
本题解析:A、2mol?L?1 KCl溶液Cl?浓度为2mol?L?1,1mol?L?1K2SO4溶液Cl?浓度也为2mol?L?1,所以2mol?L?1 KCl溶液与1mol?L?1K2SO4溶液混合后,c(K+)为2mol?L?1,正确;B、120gNaC1溶液中溶有20gNaCl,该溶液不一定是饱和溶液,错误;C、没有指明为标准状况,22.4LHCl的物质的量不确定,错误;D、CuSO4的质量小于5g,溶液的质量为50g,所得溶液溶质的质量分数小于10%,错误。
本题难度:一般
2、填空题 向橙色的溴水中通入SO2气体,观察到的现象是____________。有关的离子方程式为___________________________
参考答案:
本题解析:略
本题难度:一般
3、简答题 26.在200mL稀硫酸和稀盐酸的混合溶液中,逐滴加入1mol-L-1?Ba(OH)2溶液,当加入0.6L?Ba(OH)2时,溶液恰好中性,共得到沉淀46.6g.试求
(1)SO42-刚好沉淀完全时滴加的Ba(OH)2溶液的体积是多少?
(2)混合酸溶液中硫酸和盐酸的物质的量浓度各是多少?
参考答案:(1)向混合溶液中加入逐滴加入1mol?L-1?Ba(OH)2溶液,发生的反应是H2SO4+Ba(OH)2=BaSO4 ↓+2H2O,2HCl+Ba(OH)2=BaCl2+2H2O,得到的46.6g沉淀为BaSO4 ,BaSO4 的物质的量为46.6g233g/mol=0.2mol,根据钡离子守恒可知,n[Ba(OH)2]=n(BaSO4 )=0.2mol,故SO42-刚好沉淀完全时滴加的Ba(OH)2溶液的体积为0.2mol1mol/L=0.2L,
答:SO42-刚好沉淀完全时滴加的Ba(OH)2溶液的体积0.2L;
(2)根据硫酸根守恒可知n(H2SO4)=n(BaSO4 )=0.2mol,混合酸溶液中硫酸的物质的量浓度为0.2mol0.2L=1mol/L,
溶液恰好为中性时,溶液中溶质为BaCl2 ,根据钡离子守恒n[Ba(OH)2]=n(BaSO4)+n(BaCl2 ),
故n(BaCl2 )=n[Ba(OH)2]-n(BaSO4)=0.6L×1mol/L-0.2mol=0.4mol,由氯离子守恒有n(HCl)=2n(BaCl2 )=2×0.4mol=0.8mol,混合酸溶液中盐酸的物质的量浓度为0.8mol0.2L=4mol/L,
答:混合酸溶液中硫酸的物质的量浓度为1mol/L,盐酸的浓度为4mol/L.
本题解析:
本题难度:一般
4、选择题 下列物质书写正确的是(?)
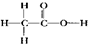
A.乙酸的结构式:
B.H2S
C.-CH3 
D.NH4I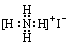
参考答案:A
本题解析:硫化氢是共价化合物,形成的化学键是极性键,电子式为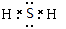 。甲基中碳原子的最外层电子是7个,电子式为
。甲基中碳原子的最外层电子是7个,电子式为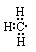 。碘化氨是离子化合物,电子式为
。碘化氨是离子化合物,电子式为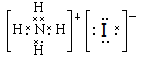 。
。
所以正确的答案是A。
本题难度:一般
5、选择题 下列关于化学用语的表示正确的是(? )
A.过氧化钠的电子式:
B.质子数为35、中子数为45的溴原子: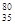 Br
Br
C.硫离子的结构示意图: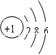
D.间二甲苯的结构简式: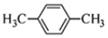
参考答案:B
本题解析:A.过氧化钠是离子化合物,电子式是: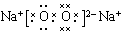 ;错误;B.符合原子的符合书写,正确;C.硫离子的结构示意图是
;错误;B.符合原子的符合书写,正确;C.硫离子的结构示意图是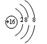 ,错误;D.间二甲苯的结构简式是:
,错误;D.间二甲苯的结构简式是: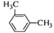 ;错误。
;错误。
本题难度:一般