��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij��Һ�к���0.005 mol FeBr2���������ʣ������Һ��ͨ��134.4 mL(��״��)Cl2����Һ��ֻ��FeBr2��Cl2��Ӧ����ͨ��Cl2����Һ�п��ܴ������ڵ�������(����)
A��Fe2����Fe3����Br����NO3-
B��Fe3����H����NO3-��K��
C��Fe3����Br����NO3-��Cl��
D��Fe2����Br����NO3-��Cl��
�ο��𰸣�C
���������0.005 mol FeBr2��134.4 mL(��״��)Cl2��Ӧ�����ӷ���ʽ�ɱ�ʾΪ��10Fe2����14Br���� 12Cl2=10Fe3����7Br2��24Cl��������Br����ʣ�࣬Fe2����ȫ�����������A��D������ȷ��B�е�H����NO3-ֻ�������ڷ�Ӧǰ����Һ���������������Ӵ������ڵ�����£�FeBr2�Dz����ܴ��ڵģ���B���ԡ�
�����Ѷȣ�һ��
2��ѡ���� ���������У���һ�������²��ܷ���ˮ�ⷴӦ��������
A.����
B.��֬
C.����
D.������
�ο��𰸣�A
���������
�����Ѷȣ���
3�������� ����FeCl3��AlCl3�Ļ����Һ100mL,��μ���NaOH��Һ�����ɳ��������ʵ���������NaOH�����ʵ����Ĺ�ϵ��ͼ��������FeCl3��AlCl3�����ʵ���Ũ�ȸ�Ϊ���٣�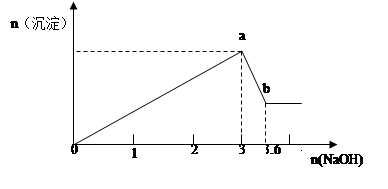
�ο��𰸣�FeCl3��AlCl3�����ʵ���Ũ�ȸ�Ϊ4mol/L��6mol/L��Ҫд���淶�ļ�����̣�
�����������Fe3+ + 3OH- = Fe(OH)3��? Al3+ + 3OH- =Al(OH)3���õ�����Fe3+�� Al3+��������ȫʱ��,�ﵽ��������a������OH-3mol����FeCl3��AlCl3��1mol
������NaOH��Al(OH)3���ܽ⣬Al(OH)3 + OH- =AlO2- +H2O
����OH-��0.6mol�����Կ�����ԭ���غ�ó�AlCl3�����ʵ���Ϊ0.6mol������FeCl3���ʵ���Ϊ0.4mol��
c(FeCl3)=n/V=0.4mol/0.1L=4mol/L��c(AlCl3)=n/V=0.6mol/0.1L=6mol/L��
�������ڴ��ܽ�һ�¶���ͼ������ķ���������(1)��������ϵ�������ݡ������������������塣(2)������㡢�յ㡢�յ㣬�������ߵı仯���ƣ���Ū���������������塣
�����Ѷȣ�һ��
4��ѡ���� �����й����ӷ���ʽ��д��ȷ��
A.��1mol FeI2��Һ��ͨ���״����22.4L Cl2��2Fe2++2I-+2Cl2�T2Fe3++I2+2Cl-
B.���������Һ��ͨ�����CO2��CH3COO-+CO2+H2O��HCO3-+2?CH3COOH
C.��NaHSO4��Һ�еμ�Ba��OH��2��Һ�����ԣ�2H++SO42-+Ba2++2OH-�TBaSO4��+2H2O
D.�Խ�����Ϊ������ⱥ������ͭ��Һ��Cu2++2H2O�T2Cu+O2��+4H+
�ο��𰸣�C
���������������A��������Һ�����ӵĻ�ԭ�ԣ�I-��Fe2+���жϷ�Ӧ������˳������Լ����ӷ���ʽ����д��
B������ǿ���������ԭ����������
C������NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����ԣ����ߵ����ʵ���֮��Ϊ2��1��
D�����ݵ��ʱ�����������ǽϻ��õĽ������ڵ�����������ʧ���ӣ��������۲�����Σ����������ӵõ��ӣ�Ȼ������ܷ�Ӧ=�����ĵ缫��Ӧ+�����ĵ缫��Ӧ��
���A������Һ�����ӵĻ�ԭ�ԣ�I-��Fe2+������Cl2������I-��Ȼ������Fe2+����1mol FeI2��Һ��ͨ���״����22.4L Cl2ʱ��ֻ��I-�����������ӷ���ʽΪ��2I-+Cl2�TI2+2Cl--����A����
B��CH3COOH�����Դ���H2CO3�����Բ�����H2CO3���Ʊ�CH3COOH����B����
C��NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����ԣ����ߵ����ʵ���֮��Ϊ2��1�����ӷ�ӦΪ2H++SO42-+Ba2++2OH-=BaSO4��+2H2O����C��ȷ��
D�����ʱ�������ĵ缫��Ӧ��2Ag++2e-=2Ag�������ĵ缫��Ӧ��Cu2++2e-=Cu�������ܷ�Ӧ��2Ag++Cu2+=2Ag+Cu����D����
��ѡC��
���������⿼�����ӷ�Ӧ����ʽ��д����ȷ�����Ļ�ѧ��Ӧ�����ӷ�Ӧ����д�������ɽ���ѶȲ���
�����Ѷȣ�����
5��ѡ���� �������ᣬ����Ũ��������С����
[? ]
A.OH-
B.HCO3-
C.SO42-
D.NO3-
�ο��𰸣�AB
���������
�����Ѷȣ���