��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���е��뷽��ʽ�������
A.HCl ��H+ +Cl-
B.Al(NO3)3��Al3+ +3NO3-
C.Na2CO3��2Na+ +CO32-
D.MgCl2��Mg2+ +Cl22-
�ο��𰸣�D
������������������DӦ��ΪMgCl2��Mg2+ +2Cl2-��
���㣺���ӷ���ʽ����д
�����Ѷȣ���
2��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����
A.�ö��Ե缫���MgCl2��Һ��2Cl-+2H2O�TCl2��+H2��+2OH-
B.���Ʒ���ˮ�⣺S2-+H2O=HS-+OH-
C.����С�մ���Һ����Ba��OH��2��Һ�У�HCO-3ʮBa2++OH-=BaCO3��+H2O
D.��NH4HSO4��Һ�м���NaOH��Һ�����ҺΪ���ԣ�H++OH-=H2O
�ο��𰸣�C
����������������������ӷ���ʽ��дҪ�����жϣ��翴�Ƿ��غ㣨��������ɡ���ʧ���ӣ����Ƿ���Ͽ���ʵ����ѧʽ��֡���ѧ����ʹ���Ƿ���ȷ����Ӧ���������䷴Ӧ�Ƿ�һ�£��Ƿ�����������ӵȣ�
���A������ʱ���������������˴���OH-��OH-����Mg2+��Ӧ��Mg2++2OH-=Mg��OH��2������A����
B����ˮ�ⷴӦΪ���淴Ӧ��S2-��ˮ���á�?�������á�=������B����
C����HCO-3+OH-=CO32-+H 2O����������С�մ���Һ����Ba��OH��2��Һ�з���NaHCO3+Ba��OH��2=BaCO3��+H2O+NaOH����C��ȷ��
D����NH4HSO4��Һ��NH+4��OH-��Ӧ��NH+4+OH-=NH3?H2O����D����
��ѡC��
���������⿼�������ӷ���ʽ�����жϵķ�����ֻҪ����һЩ�������жϷ������Ϳ�������ӭ�ж����ˣ�
�����Ѷȣ�һ��
3��ʵ���� ʵ������Na2SO3������70�������ᷴӦ��ȡSO2����ʱ������FeC13��Һ���ն����SO2���塣
��1��д��SO2��FeC13��Һ��Ӧ�����ӷ���ʽ��?��
��2��FeC13��Һ����SO2����һ��ʱ�������Һ��һ�����ڵ������У�H+��Fe2+��C1����SO42-��ijͬѧ��Ϊ�����ܴ����������ӣ�������������ʵ��̽����
������������裺
����1��������HSO3-��SO32-
����2��������Fe3+
����3��HSO3-��SO32-��Fe3+��������
�����ʵ�鷽��
ʵ�鲽��
| ����ͽ���
|
����1��ȡ��������Һ���Թܣ��μ�ϡ�����ữ��Ȼ���ٵ��뼸��?��Һ��
| ����?
���ۣ�����1��������
|
����2��?
?
| ����?
���ۣ�����2������
|
?
��3���ⶨ������SO2�����ķ����ǣ���500L��SO2����Ŀ���ͨ��20mL��0.00015molKMnO4����Һ�У���ַ�Ӧ������0.02000mol/L��KI��Һ�ζ�������KMnO4������KI ��Һ25.00mL��������е�SO2����Ϊ?mg/L��
��5SO2+2MnO4-+2H2O��2Mn2++5SO42-+4H+��10I��+2MnO4-+16H+��2Mn2++5I2+8H2O��
�ο��𰸣�
��1��SO2+2Fe3++2H2O=SO42��+2Fe2++4H+
��2������Ʒ����Һ?Ʒ�첻��ɫ?ȡ��������Һ���Թܣ��μ�����KSCN��Һ?��Һ���?
��3��0.016mg/L
�������������Fe3+�������Ժ�+4��S�Ļ�ԭ��֮�䷢����Ӧ�IJ������̽��������SO32-��HSO3-��Fe2+��Fe3+�ļ��飬SO32-��HSO3-������ת��ΪSO2��ͨ��Ʒ����Һ�����飬Fe3+���飬������KSCN�����顣���ݷ�Ӧ10I��+2MnO4-+16H+��2Mn2++5I2+8H2O���������������ص����ʵ���Ϊ ��0.02000mol/L��0.025L=0.0001mol����֪������һ����Ӧ�����ĵĸ��� ���Ϊ0.00015mol-0.0001mol=5��10-5mol��n(SO2)= 1.25��10-4mol������Ϊ1.25��10-4mol��64g/mol/500L=0.16��10-4g/L=0.016mg/L��
��0.02000mol/L��0.025L=0.0001mol����֪������һ����Ӧ�����ĵĸ��� ���Ϊ0.00015mol-0.0001mol=5��10-5mol��n(SO2)= 1.25��10-4mol������Ϊ1.25��10-4mol��64g/mol/500L=0.16��10-4g/L=0.016mg/L��
�����Ѷȣ�һ��
4��ѡ���� ��֪�ڳ����£����Ũ�Ⱦ�Ϊ0.1?mol/L������������Һ��pH
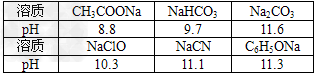
���ֽⷴӦ����һ�����ɣ����Խ�ǿ�����ʷ������Ʒ�Ӧ�������ɼ��Խ��������ʡ����ոù��ɣ������ж��������ӷ�Ӧ���ܳ�������
[? ]
A��CO32����C6H5OH��HCO3����C6H5O��
B��CO2��H2O��ClO��===HCO3����HClO
C��CO2��H2O��C6H5O����HCO3����C6H5OH
D��CO2��H2O��2C6H5O����CO32����2C6H5OH
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ���и���������ָ���������ܴ����������
A.��pH=0����Һ�У�Cu2+��Al3+��SO42-��NO3-
B.��ɫ��Һ�У�K+��Ag+��CO32-��Br-
C.��ˮ�������c(H+)��1��10-13 mol/L����Һ�У�Na+��Mg2+��Cl-��HCO3-
D.���д��� Fe3+����Һ�У�NH4+��Na+��I-��SCN-
�ο��𰸣�A
�����������ȷ�𰸣�A
B.��ɫ��Һ�У� Ag+��CO32-��Br-�����棻
C.��ˮ�������c(H+)��1��10-13 mol/L����Һ�����������Ի���ԣ� HCO3-��������
D.���д��� Fe3+����Һ�У� I-��SCN-�����ܹ��档
�����Ѷȣ�һ��