微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在托盘天平两边托盘上分别放置盛有足量的体积相等、溶质质量分数相等的盐酸的烧杯,使天平处于平衡状态,现向烧杯分别加入等质量纯碱和小苏打,充分反应后,天平指针
A.向加小苏打的一端偏
B.向加纯碱的一端偏
C.不偏转
D.无法确定如何偏转
参考答案:B
本题解析:分析:因的盐酸质量相等,所以需要判断两端加入一定量物质后增加质量是否相等.
若增加质量相等时天平能仍然保持平衡,若不相等时天平发生偏转.
假设加入的质量为106g,盐酸足量,加入的盐完全反应,根据化学方程式,借助关系式和差量法进行分析比较质量变化.
解答:根据化学方程式,利用关系式法计算加入碳酸钠,溶液质量的变化.
Na2CO3~CO2↑? 溶液质量增加(△m)
106? 44? 62
106g? 62g
根据化学方程式,利用关系式法计算加入碳酸氢钠,溶液质量的变化.
NaHCO3~CO2↑? 溶液质量增加(△m)
84? 44?40
106g? m
m=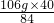 =50.5g
=50.5g
?所以加入碳酸钠一端溶液质量增重大,故天平指针向加纯碱的一端偏.
故选B.
点评:本题考查天平平衡原理,难度中等,关键明白若增加质量相等时天平能仍然保持平衡,若不相等时天平发生偏转.
本题难度:一般
2、选择题 下列气体通入水中,所得溶液呈碱性的是
A.Cl2
B.NO2
C.CO2
D.NH3
参考答案:D
本题解析:由Cl2+H2O=HCl+HClO? 3NO2+H2O=2HNO3+NO? CO2+H2O=H2CO3知,所得溶液均呈酸性,而氨气为碱性气体,溶于水得到弱碱一水合氨,符合题意
本题难度:简单
3、选择题 下列物质转化在给定条件下不能实现的是
A.Fe2O3FeCl3(aq)无水FeCl3
B.Al2O3NaAlO2(aq)AlCl3
C.NH3NOHNO3
D.饱和NaCl(aq)NaHCO3Na2CO3
参考答案:A
本题解析:分析:A、氧化铁与盐酸反应生成氯化铁,Fe3+水解,加热蒸发得不到无水FeCl3;
B、氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液加入盐酸,生成氯化铝;
C、氨气的催化氧化会生成一氧化氮,一氧化氮易被氧化为二氧化氮,二氧化氮溶于水中得到硝酸;
D、在饱和食盐水中通入氨气,形成饱和氨盐水,再向其中通入二氧化碳,在溶液中就有了大量的钠离子、铵根离子、氯离子和碳酸氢根离子,其中NaHCO3溶解度最小,所以析出NaHCO3,加热NaHCO3分解生成碳酸钠.
解答:A、氧化铁与盐酸反应生成氯化铁,Fe3+水解Fe3++3H2O?2Fe(OH)3+HCl,加热蒸发HCl挥发,平衡向右移动,得不到无水
FeCl3,故A选;
B、氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液加入盐酸,生成氯化铝,故B不选;
C、氨气的催化氧化会生成一氧化氮,一氧化氮易被氧化为二氧化氮,二氧化氮溶于水中得到硝酸,故C不选;
D、在饱和食盐水中通入氨气,形成饱和氨盐水,再向其中通入二氧化碳,在溶液中就有了大量的钠离子、铵根离子、氯离子和碳酸氢根离子,其中NaHCO3溶解度最小,析出NaHCO3,加热NaHCO3分解生成碳酸钠,故D不选.
故选A.
点评:本题考查学生元素化合物、侯氏制碱法、盐类的水解等方面的知识,注意知识的梳理和归纳是解题的关键,难度不大.
本题难度:困难
4、选择题 下列离子方程式错误的是
A.用Na2CO3溶液作洗涤剂:CO32-+2H2O?H2CO3+2OH-
B.用铜作电极电解氢氧化钠溶液:2H2O?2H2↑+O2↑
C.“银镜反应”:RCHO+2Ag(NH3)2++2OH-?2Ag+RCOO-+NH4++3NH3+H2O
D.交警用酸化的含Cr2O72-的硅胶检测司机酒后驾驶的反应:2Cr2O72-+3C2H5OH+16H+→4Cr3++3CH3COOH+11H2O
参考答案:AB
本题解析:分析:A、碳酸根离子是多元弱酸阴离子分步水解;
B、电解池中铜做阳极铜失电子发生氧化反应;
C、醛基被银氨溶液氧化为醋酸,结合氨气生成醋酸铵;
D、重铬酸根离子具有强氧化性能氧化乙醇为乙酸,本身颜色变化.
解答:A、用Na2CO3溶液作洗涤剂,因为碳酸根离子水解显碱性:CO32-+H2O?HCO3-+OH-;HCO3-+H2O?H2CO3+2OH-,故A错误;
B、用铜作电极电解氢氧化钠溶液,铜做阳极是活性电极,铜失电子发生氧化反应:Cu+2H2O? ?2H2↑+Cu(OH)2↓,故B错误;
?2H2↑+Cu(OH)2↓,故B错误;
C、醛基被银氨溶液氧化为醋酸,结合氨气生成醋酸铵;“银镜反应”的离子方程式为:RCHO+2Ag(NH3)2++2OH-?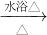 ?2Ag+RCOO-+NH4++3NH3+H2O,故C正确;
?2Ag+RCOO-+NH4++3NH3+H2O,故C正确;
D、重铬酸根离子具有强氧化性能氧化乙醇为乙酸,本身颜色变化,反应的离子方程式为:2Cr2O72-+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O,故D正确;
故选AB.
点评:本题考查离子方程式的书写方法和注意问题,反应实质的理解和掌握是解题关键,题目难度中等.
本题难度:简单
5、选择题 把CO2通入NaOH溶液中,当生成Na2CO3和NaHCO3的物质的量之比为2:1时,CO2和NaOH的物质的量之比为
A.3:2
B.3:4
C.3:5
D.1:2
参考答案:C
本题解析:本题可直接用“钠离子和碳原子守恒”来做。设Na2CO3和NaHCO3的物质的量分别为2mol、1mol。则钠离子的物质的量为2mol×2+1mol=5mol;碳原子的物质的量为2mol+1mol=3mol。显然,CO2和NaOH的物质的量之比为3:5。
本题难度:困难