微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 我国多地已发生误食亚硝酸盐中毒事件。人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐,则导致血红蛋白中Fe2+转化为高价铁,使血红蛋白中毒。服用维生素C可解除亚硝酸盐中毒。在维生素C解毒的反应中,正确的说法是(? )
A.亚硝酸盐是还原剂
B.维生素C将Fe3+还原为Fe2+
C.维生素C是氧化剂
D.亚硝酸盐被还原
参考答案:B
本题解析:由于人体血红蛋白中的Fe2+被亚硝酸盐氧化为Fe3+,维生素C的解毒作用利用了其还原性,将Fe3+还原为Fe2+。
本题难度:一般
2、选择题 把钠放入滴有石蕊试液的水中,下列现象不易观察到的是(?)
A.钠浮在水面上
B.溶液中产生较多气泡
C.水溶液变为蓝色
D.钠熔化成小球并在水面游动
参考答案:B
本题解析:略
本题难度:一般
3、实验题 工业生产纯械的工艺流程示意图如下

完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(A来源于石灰窑厂),则B的化学式_________。
(2)②过滤后滤液中要通入C和D气体,则先通入的C气体是_________(填化学式),原因是_________。
(3)通入C和D气体后发生反应的化学方程式是_________。
(4)④过滤后,向滤液中通氨气,加入细小食盐颗粒,析出副产品________ (填写化学式),通氨气与加入细小食盐颗粒的作用是_________。
(5)写出⑤锻烧发生反应的化学方程式_________。产品纯碱中含有碳酸氢钠,若用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质童分数ω(NaHCO3)= _________ (注明表达式中所用的有关符号的含义)。
参考答案:(每空2分,第(1)问1分,共计15分)(1)Na2CO3
(2)NH3;因为在CO2水中的溶解度小,而NH3溶解度大
(3)NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
(4)NH4Cl;增大溶液中的Cl-、NH4+的浓度,降低NH4Cl的溶解度,使NH4Cl大量析出
(5)2NaHCO3 Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O; 
本题解析:(1)粗盐提纯时需要除去的杂质离子是Ca2+、Mg2+,A来源于石灰窑厂,则A是生石灰或熟石灰,用来除去Mg2+,而Ca2+一般用碳酸钠来除去,即B试剂是碳酸钠。
(2)由于在CO2水中的溶解度小,而NH3溶解度大,所以要先通入氨气,然后再通入CO2气体。
(3)由于碳酸氢钠的溶解度较小,所以向氨气饱和的氯化钠溶液中通入CO2气体会产生碳酸氢钠晶体,反应的化学方程式是NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(4)由于溶液中含有氯离子和NH4+,所以加入细小食盐颗粒,增大溶液中的Cl-、NH4+的浓度,降低NH4Cl的溶解度,使NH4Cl大量析出,因此析出副产品是氯化铵。
(5)碳酸氢钠稳定性差,在加热的条件下能发生分解,反应的化学方程式为2NaHCO3 Na2CO3+CO2↑+H2O;假设加热前纯碱的质量为m(加热前),加热后的质量为m(加热后),则加热损失的质量为[m(加热前)-m(加热后)],因此根据方程式可知,纯碱中碳酸氢钠的质量为
Na2CO3+CO2↑+H2O;假设加热前纯碱的质量为m(加热前),加热后的质量为m(加热后),则加热损失的质量为[m(加热前)-m(加热后)],因此根据方程式可知,纯碱中碳酸氢钠的质量为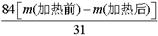 ,所以纯碱中含有的碳酸氢钠的质量分数为
,所以纯碱中含有的碳酸氢钠的质量分数为 。
。
本题难度:一般
4、选择题 将过氧化钠和过量的碳酸氢钠在密闭容器中混合充分加热后,最终残留固体物质是
A.Na2CO3
B.Na2O和Na2O2
C.Na2O2
D.Na2O2和Na2CO3
参考答案:A
本题解析: 2NaHCO?=Na2CO?+ CO2↑+ H2O
2Na2O2 + 2CO2 ="===" 2Na2CO3 +O2↑
2Na2O2+2H2O ="===" 4NaOH + O2↑
2NaOH + CO2 ="===" Na2CO3+H2O
由以上反应式可知:由于碳酸氢钠是过量的,所以产物中一定不会有过氧化钠,故选A。
点评:熟悉常见的化合物之间的反应,此类问题考查的就是学生对基本知识的掌握程度。
本题难度:简单
5、选择题 在一个可以加热的密闭容器中,加入Na2O2和NaHCO3各0.5mol,将容器加热至400℃,待充分反应后排出气体,则容器中剩余的固体是
A.Na2CO3
B.Na2CO3和Na2O2
C.NaOH
D.Na2CO3和NaOH
参考答案:D
本题解析:①2NaHCO3=Na2CO3+H2O↑+CO2↑
②2Na2O2+2CO2=2Na2CO3+O2?②2Na2O2+2H2O=4NaOH+O2?
根据反应式可计算出,NaHCO3完全分解生成Na2CO3,而生成的气体CO2、H2O依次与Na2O2恰好完全反应生成Na2CO3与 NaOH,故最终剩余固体为Na2CO3和NaOH
本题难度:一般