微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 铁是人体必需的微量元素,如果人长期缺铁,会引起缺铁性贫血,导致某些疾病,如口角炎与舌炎、萎缩性胃炎与胃酸缺乏、皮肤干燥、角化和萎缩、毛发易折与脱落、指甲不光整、扁平甲、反甲和灰甲等症状。常见的治疗方法是服用补铁药物,市场上一种常见的药物其商品名称为:速力菲,药品正式名称为:琥珀酸亚铁薄膜片,本品为黄棕色薄膜衣片,除去薄膜衣后显暗黄色,药片中Fe2+的含量为34.0%~36.0%。该药片在水和乙醇中溶解度不大。现某学校化学实验小组,为了检测“速力菲”药片中亚铁元素 的存在,设计了如下几组实验:
理论设计方案:
 ?
?
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果,请你分析,可能的原因是什么?
(1)甲组实验失败的原因__________________________________;
乙组同学认真思考了甲组实验失败的原因,模拟药片服用后在人体中溶解的变化过程,重新设计并完成下列实验:
 ?
?
(2)试剂1为______________________,
试剂2为______________________,加入试剂2后,溶液为什么显示淡红色?___________________________, 加入双氧水溶液后,为什么红色加深?_________________________________________,产生的气体可能是_________________________,写出产生气体的化学方程式:_____________________________。
参考答案:(1)该药片在水中溶解度不大,少量溶解后的溶液中几乎不存在Fe2+,所以得不到预期的实验现象
(2)盐酸;KSCN溶液;在溶解过程中有少量Fe2+已经氧化成Fe3+,与SCN-结合成浓度较小的红色[Fe(SCN)]3+络离子;加入的H2O2能将Fe2+氧化为Fe3+,导致溶液中Fe3+浓度增大,[Fe(SCN)]2+络离子浓度也随之增大,所以红色加深;氧气;2H2O2 2H2O+O2↑
2H2O+O2↑
本题解析:
本题难度:一般
2、选择题 不活泼金属不能与非氧化性酸发生自发的置换反应,但某学生喜欢探究欲完成
2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的实验是?(?)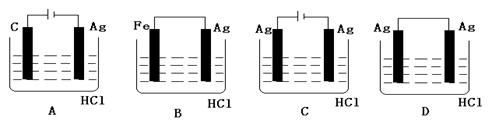
参考答案:C
本题解析:略
本题难度:一般
3、选择题 要使含Ag+、Cu2+、Mg2+、Ba2+、Al3+的溶液中各离子逐一形成沉淀析出,下列所选择的试剂和加入试剂的顺序均正确的是( )
A.H2SO4→HCl→K2S→NaOH→CO2
B.NaCl→Na2SO4→Na2S→Na2OH→CO2
C.NaCl→Na2SO4→NaS→NH3?H2O→HCl
D.Na2S→Na2SO4→NaCl→NaOH→CO2
参考答案:A.先加入硫酸,可生成硫酸银、硫酸钡沉淀,故A错误;
B.可依次生成AgCl、BaSO4、CuS、Cu(OH)2、Al(OH)3等沉淀,符合题目要求,故B正确;
C.加入硫化钠之后加入氨水可同时生成氢氧化铝和氢氧化镁沉淀,故C错误;
D.先加入硫化钠,可同时生成硫化银、硫化铜、氢氧化铝(水解生成)等沉淀,故D错误.
故选B.
本题解析:
本题难度:一般
4、选择题 能把K2SO4、Ba(NO3)2、Na2CO3三种无色溶液鉴别出来的一种试剂是( )
A.KNO3溶液
B.稀硫酸
C.NaOH溶液
D.Na2SO4溶液
参考答案:A、硝酸钾和K2SO4、Ba(NO3)2、Na2CO3三种无色溶液混合时,均没有现象发生,故A错误;
B、硫酸和硫酸钾不反应,和硝酸钡反应生成白色沉淀,和碳酸钠反应生成气体,现象不同,故B正确;
C、氢氧化钠和和K2SO4、Ba(NO3)2、Na2CO3三种无色溶液混合时,均没有现象发生,故C错误;
D、硫酸钠只会和硝酸钡反应生成白色沉淀,但是和硫酸钾以及碳酸钠均不反应,无法鉴别二者,故D错误.
故选B.
本题解析:
本题难度:一般
5、简答题 (10分)活性氧化锌用途非常广泛。以氧化锌粗品(含铁的氧化物、CuO和SiO2等杂质)为原料制备活性氧化锌并生产其它副产品的生产工艺流程如下:

已知:Zn(OH)2可溶于NaOH溶液。
请回答下列问题:
(1)“溶解”前将氧化锌粗品粉碎成细颗粒,其目的是?。
(2)操作A所得滤渣的主要成分是?。
(3)加入过量Fe时,滤液M中与Fe反应的离子有?。
(4) 操作C所得的滤渣P中含有Fe(OH)2和Fe(OH)3,请写出生成Fe(OH)3的化学反应方程式为?。
(5)“沉淀”的成分为ZnCO3・2Zn(OH)2・H2O,可用氧化物的形式把它改写为?。
参考答案:(1)增大接触面积使其能充分反应(2分)(2)SiO2(2分)。
(3)H+、Cu2+、Fe3+(2分)。?(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3(2分)
(5)3ZnO・CO2・3H2O(2分)
本题解析:根据题给信息和化学工艺流程知,氧化锌粗品(含铁的氧化物、CuO和SiO2等杂质)在稀硫酸中溶解生成硫酸铜、硫酸锌、硫酸铁和硫酸亚铁,经操作A过滤,滤渣的成分为二氧化硅;向滤液M中加入过量铁,铁与硫酸铁反应生成硫酸亚铁,铁与硫酸铜反应生成硫酸亚铁和铜,过滤得滤渣铁和铜的混合物,滤液N为硫酸亚铁和硫酸锌的混合物;向滤液N中加过量氢氧化钠溶液,铁元素转化为氢氧化物沉淀,过滤,滤渣P含有Fe(OH)2和Fe(OH)3,滤液Q酸化后加入碳酸钠溶液,锌元素转化为沉淀,煅烧得氧化锌。(1)“溶解”前将氧化锌粗品粉碎成细颗粒,其目的是增大接触面积使其能充分反应;(2)由上述分析知,操作A所得滤渣的主要成分是SiO2;(3)加入过量Fe时,滤液M中与Fe反应的离子有H+、Cu2+、Fe3+;(4)Fe(OH)2与氧气、水反应生成Fe(OH)3的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3; (5)“沉淀”的成分为ZnCO3・2Zn(OH)2・H2O,可用氧化物的形式把它改写为3ZnO・CO2・3H2O。2等杂质)为原料制备活性氧化锌并生产其它副产品的生产工艺流程为载体考查物质的分离提纯、化学方程式的书写及阅读材料接受信息的能力。
本题难度:一般