微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 根据从草木灰中提取钾盐的实验,填写下列空白:
(1)此实验操作顺序如下:①称量样品,②溶解、沉降, ③____,④____,⑤冷却、结晶。
(2)用托盘天平(指针向上的)称量样品时,若指针偏向右 边,则表示____(填下列正确选项的代码)。 A.左盘重,样品轻 B.左盘轻,砝码重 C.右盘重,砝码轻 D.右盘轻,样品重
(3)在进行第③步操作时,有可能要重复进行,这是由于___ 。
(4)在进行第④步操作时,要用玻璃棒不断小心地搅动液体,目的是防止____。
(5)所得产物中主要的钾盐有____等。
参考答案:(1)③过滤 ;④蒸发浓缩
(2)B
(3)滤液浑浊
(4)液体飞溅
(5)K2CO3、K2SO4、KCl等
本题解析:
本题难度:一般
2、实验题 为了探究铜与浓硫酸的反应,某研究性学习小组做了如下实验
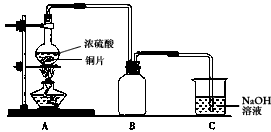
①在放有铜片的圆底烧瓶中加入10mL浓硫酸,加热煮沸10min(如图所示)后,所得固体分离除去未反应的铜片,再经水洗仍有大量黑色不溶物。
②取少量不溶物,向其中加入几滴浓硝酸,产生大量红棕色气体。
③取少量不溶物,向其中加5mL酒精,充分振荡后,静置、过滤,把滤液移入盛有水的小试管中,振荡,出现浑浊。
④取少量不溶物,向其中加入3mL氨水,振荡,溶液呈无色,在空气中静置,溶液变为深蓝色。
⑤取少量不溶物,向其中加入浓盐酸并加热,沉淀几乎全部溶解。为了解释上述现象,学习小组通过查阅资料了解到。
a.铜与浓硫酸反应的不溶性副产物可能有:CuS、Cu2S、Cu2O、S等物质;
b.CuS和Cu2S都能溶于热的浓盐酸;
c.Cu2O能溶于氨水生成无色的[Cu(NH3)2]+,[Cu(NH3)2]+在氨水中被空气中的氧气氧化成深蓝色的
[Cu(NH3)4]2+。
回答下列问题:
(1)实验结束后,装置C中的溶液中可能含有的溶质有__________________。
(2)第②步操作要注意的问题是_________________________;对比①②两步操作中的现象,你能得到的结论是_________________________。
(3)第③步操作中出现的沉淀是__________________,请解释出现这一现象的原因_______________。
(4)写出④步涉及的离子方程式______________________________。
(5)综合分析铜与浓硫酸的反应,生成的不溶物是___________________________。
(6)某工厂拟用废铜屑制备硫酸铜,请你分析利用上述实验原理是否可行。若可行,请说明理由____________________________________。若不可行,请设计更合理的实验方案(用化学反应方程式表示)
______________________________。
参考答案:(1)Na2SO3、NaOH、Na2SO4
(2)必须在密闭系统中(或在通风厨中)进行,防止污染空气(或防止中毒);黑色沉淀中有还原性物质,浓硝酸的氧化性强于浓硫酸。
(3)硫(或S);硫微溶于酒精但不溶于水,将硫的酒精溶液倒入水中,即可析出固体硫
(4)Cu2O+4NH3・H2O=2[Cu(NH3)2]++2OH-+3H2O,4[Cu(NH3)2]++8NH3・H2O+O2=4[Cu(NH3)4]2++4OH-+
6H2O
(5)Cu2O、S以及CuS和Cu2S中的一种或两种
(6)“略”
本题解析:
本题难度:困难
3、实验题 甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
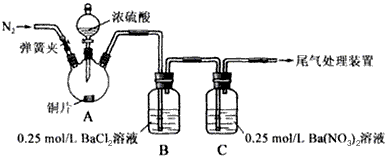
|
实验操作和现象
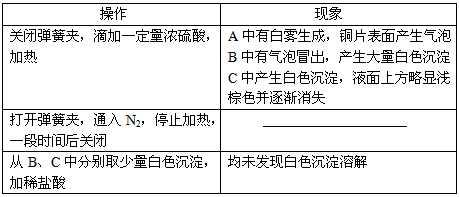
⑴A中反应的化学方程式是_______________。
⑵C中白色沉淀是__________,该沉淀的生成表明SO2具有____________性。
⑶C中液面上方生成浅棕色气体的化学方程式是____________________________。
⑷分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是______________;乙在A、B间增加洗气瓶D,D中盛放的试剂是______________。
②进行实验,B中现象
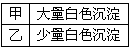
检验白色沉淀,发现均不溶于稀盐酸。结合离子方程式解释实验现象异同的原因:______________。
⑸合并⑷中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是____________________________。
参考答案:⑴Cu+2H2SO4 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
⑵H2SO4;还原
⑶2NO+O2==2NO2
⑷①通N2一段时间,排除装置中的空气;饱和NaHSO3溶液;②甲:SO42-+Ba2+==BaSO4↓,
乙:2Ba2++2SO2+O2+2H2O==2BaSO4↓+4H+,白雾的量远多于装置中O2的量
⑸SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
本题解析:
本题难度:困难
4、选择题 只用一种试剂可区别四种溶液Na2SO4、FeCl2、Al2(SO4)3、(NH4)2SO4,此试剂是( )
A.BaCl2溶液
B.稀H2SO4
C.NaOH浓溶液
D.AgNO3溶液
参考答案:A.因Na2SO4、Al2(SO4)3、(NH4)2SO4与BaCl2溶液反应均生成白色沉淀,现象相同,不能区别,故A错误;
B.四种物质与稀硫酸均不反应,现象相同,不能区别,故B错误;
C.Na2SO4、FeCl2、Al2(SO4)3、(NH4)2SO4分别与NaOH溶液反应的现象为:无现象、白色沉淀迅速变为灰绿色最后变为红褐色、白色沉淀后溶解、有刺激性气味的气体,现象不同,能区别,故C正确;
D.四种物质与AgNO3溶液反应均生成白色沉淀,现象相同,不能区别,故D错误;
故选C.
本题解析:
本题难度:一般
5、选择题 下列化学实验事实及其解释都正确的是?(?)
A.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝
B.将SO2通入含HClO的溶液中,生成H2SO4,说明HC1O酸性比H2SO4强
C.FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活动性大于Cu
D.乙烯和苯都能使溴水褪色,说明乙烯和苯都能和溴水发生加成反应
参考答案:A
本题解析:A:正确
B:错误,两者反应是氧化还原反应,次氯酸将SO2氧化为硫酸
C:FeCl3溶液可以腐蚀线路板上的Cu,本质是氧化还原反应,只能说明铁离子的氧化性强于铜离子
D:乙烯可和溴水发生加成反应,但苯只是萃取了溴水中的溴,是物理过程
答案为A
本题难度:一般