微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)  ?Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
?Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
A.达到平衡时X浓度为0.04 mol/L
B.将容器体积变为20 L,Z的平衡浓度变为0.015mol/L
C.若增大压强,平衡向正方向移动,平衡常数变大
D.若升高温度,X的体积分数增大,则该反应的DH>0
参考答案:A
本题解析:生成0.3 mol Z,则消耗X是0.6mol,所以剩余X是0.4mol,浓度是0.04mol/L,A正确。将容器体积变为20 L,则压强降低,平衡向逆反应方向移动,因此Z的平衡浓度小于0.015mol/L,B不正确。平衡常数只与温度有关系,所以选项C不正确。升高温度,X的体积分数增大,说明平衡向逆反应方向移动,因此正反应是放热反应,D不正确,答案选A。
本题难度:一般
2、选择题 在某一化学反应中,反应物A的浓度在20 s内从1.0 mol/L变为0.2 mol/L,则在这20 s内以A浓度的变化表示的平均反应速率为
A.0.04 mol / (L・s)
B.0.04 mol / L
C.0.08 mol / (L・s)
D.0.08 mol / L
参考答案:A
本题解析:试题分析:反应速率通常用单位时间内浓度的变化量来表示,则以A浓度的变化表示的平均反应速率为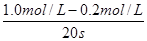 =0.04 mol / (L・s),答案选A。
=0.04 mol / (L・s),答案选A。
考点:考查反应速率的计算
点评:该题是高考中的常见考点,属于常识性知识的考查。该题的关键是明确反应速率的含义以及计算依据,有利于培养学生的逻辑推理能力和规范答题能力。
本题难度:简单
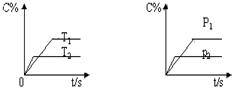
3、选择题 右图表示可逆反应mA(g)+nB(g) pC(g)在不同温度(T)、压强(P)下,生成物C的质量分数C%的变化情况。下列关于该正反应热效应及方程式中A. B. C的化学计量数的判断中,正确的是
pC(g)在不同温度(T)、压强(P)下,生成物C的质量分数C%的变化情况。下列关于该正反应热效应及方程式中A. B. C的化学计量数的判断中,正确的是
A.吸热反应,m+n<p? B.吸热反应,m+n>p
C.放热反应,m+n<p? D.放热反应,m+n>p
参考答案:C
本题解析:根据图像可知,温度为T2时反应首先达到平衡状态,则T2大于T1。温度高C的百分含量低,这说明升高温度平衡逆反应方向移动,因此正反应是放热反应;同样分析可知,压强为P2时反应首先达到平衡状态,则P2大于P1。压强高C的百分含量低,这说明增大压强平衡逆反应方向移动,因此正反应是体积增大的可逆反应,即m+n<p,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,旨在考查学生灵活运用基础知识解决实际问题的能力。该类试题需要明确的是在分析有关图像时应该注意:一、ν-t 图像或 c-t 图像:1.ν-t 图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。?二、平衡图像 1.出现拐点的图像:分析依据“先拐先平”。在转化率-时间图像或物质的百分含量-时间图像中,先出现拐点的曲线先达到平衡(代表温度高或压强大或使用合适的催化剂等)。
本题难度:一般
4、填空题 (1) 反应: 2A(g)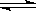 B(g ) xC(g) 在一定的条件下达到平衡状态, 密闭容器中的压强增大P%, 测得A的转化率为 P%, 则x的值为 __________.
B(g ) xC(g) 在一定的条件下达到平衡状态, 密闭容器中的压强增大P%, 测得A的转化率为 P%, 则x的值为 __________.
(2) 在容积相同的两密闭容器A和B中, 保持温度为 423K, 同时向A和B中分别加入 a mol 和 b mol 的HI(a > b), 待反应: 2HI(g)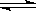 H2(g)+ I2(g)到平衡后, 用 “ > < 或 ="”" 回答下列问题:
H2(g)+ I2(g)到平衡后, 用 “ > < 或 ="”" 回答下列问题:
从反应开始到达到平衡所需要时间: tA _______ tB(填>,<, =",?" 下同)
平衡时的碘的浓度: c(I2 )A?c(I2 )B
HI的平衡分解百分率为:  .
.
参考答案:(1)? 3? (2)<? ,>? ,=
本题解析:略
本题难度:简单
5、填空题 在一定温度下,在10L密闭容器中加入5molSO2和一定量的氧气,在一定条件下发生反应: 2SO2(g)+O2(g) 2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
(1)氧气的起始浓度为?。
(2)平衡时剩余SO2??mol;
(3)该条件下SO2的最大转化率为?;
(4)平衡时体系中SO3的百分含量(体积分数)为 ?;
(5)平衡体系中SO2、O2和SO3的物质的量之比为?。
参考答案:(5分)(1)0.5mol/L;(2)1; (3)80%;(4)50%;(5)1:3:4
本题解析:? 2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
起始浓度(mol/L)? 0.5? x? 0
转化浓度(mol/L)? 0.4? 0.2? 0.4
平衡浓度(mol/L)? 0.1? 0.3? 0.4
所以氧气的起始浓度为0.2mol/L+0.3mol/L=0.5mol/L
平衡时剩余SO2的物质的量是0.1mol/L×10L=1mol
该条件下SO2的最大转化率为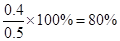
平衡时体系中SO3的百分含量(体积分数)为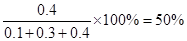
平衡体系中SO2、O2和SO3的物质的量之比为0.1:0.3:0.4=1:3:4
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。
本题难度:一般