微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列变化一定要加入还原剂才能实现的是( )
A.KMnO4→K2MnO4
B.HCl→Cl2
C.H2SO4(稀)→H2
D.Na2O→NaOH
参考答案:C
本题解析:
本题难度:一般
2、简答题 .用KMnO4氧化密度为1.19g/cm3,溶质的质量分数为36.5%的?盐酸.反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出上述反应电子得失数目.
(2)求所用盐酸的物质的量浓度.
(3)15.8gKMnO4能使多少克HCl发生上述反应?产生的Cl2在标准状况下的体积为多少?
参考答案:(1)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,Mn元素的化合价+7→+2,和Cl元素的化合价-1→0,反应中氧化剂和还原剂得失电子数目相等,
答:双线桥法标出反应中电子得失数目为
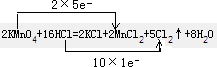
;
(2)c(HCl)=1000ρwM=1000×1.19×36.5%36.5=11.9(mol?L-1),
答:所用盐酸的物质的量浓度为11.9mol?L-1;
(3)设15.8gKMnO4能同xgHCl发生反应,生成标准状况下yLCl2.
? 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
2×158?g?16×36.5?g?5×22.4?L
?15.8?g? x?g? y?L
则?x=16×36.5×15.82×158=29.2?(g),
y=5×22.4L×15.8g2×158g=5.6L.
答:15.8gKMnO4能使29.2克HCl发生上述反应;产生的Cl2在标准状况下的体积为5.6L.
本题解析:
本题难度:一般
3、填空题 分类法对研究化学物质和化学反应有重要的意义,请完成下列问题.
(1)今有八种物质:①铝?②熔化的KNO3?③石墨?④NaCl晶体?⑤纯硫酸? ⑥石灰水?⑦乙醇?⑧BaSO4固体
其中能导电的物质是______,属于电解质的是______.
(2)下列4组物质均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO? ?B.H2、C、P、Cu
C.O2、Fe、Cu、Zn?D.HCl、H2O、H2SO4、HNO3
以上四组物质中与别不同的物质依次是(填化学式)
A______;B______;C______;D______.
(3)写出一个水既不作氧化剂又不作还原剂但反应中有电子转移的化学反应方程式,利用双线桥分析电子转移方向和数目,并指出氧化剂和还原剂.
参考答案:(1)①铝是金属单质,能导电;但它既不是电解质也不是非电解质;?
②熔化的KNO3电离出自由移动的钾离子和硝酸根离子,能导电;它是化合物,属于电解质;
③石墨是非金属单质,能导电;但它既不是电解质也不是非电解质;
④NaCl晶体在熔融状态下以及其溶液有自由移动的钠离子和氯离子,能导电;它是化合物,属于电解质;
⑤纯硫酸只存在硫酸分子不导电;硫酸水溶液能导电,为自身完全电离出的自由移动的氢离子和硫酸根离子,所以硫酸是电解质;
⑥石灰水溶液中有自由移动的钙离子和氢氧根离子,能导电;但氢氧化钙溶液,是混合物,所以,它既不是电解质也不是非电解质;
⑦乙醇是化合物,但其水溶液只存在乙醇分子,不导电,属于非电解质;
⑧BaSO4固体没有自由移动的离子不导电;?虽然硫酸钡在水中的溶解度很小,只要溶解就完全电离,硫酸钡在熔融状态下,能完全电离,所以硫酸钡是电解质;
故答案为:①②③⑥,②④⑤⑧;
(2)A.CaO、Na2O、K2O均是金属氧化物,而CO2为非金属氧化物;
B.H2、N2、P是非金属元素组成的单质分子,而Cu均是金属元素组成的单质;
C.Fe、Cu、Zn是金属元素组成的单质,而O2是非金属元素组成的单质分子;
D.HCl、H2SO4、HNO3均是酸,而H2O是氧化物;
故答案为:A.?CO2;?B.?Cu;?C.?O2;?D.?H2O;
(3)反应3NO2+H2O=2HNO3+NO中,二氧化氮氮元素化合价既升高也降低,二氧化氮既作氧化剂又作还原剂,水中H和O元素的化合价不变,水既不作氧化剂又不作还原剂,3mol的NO2中,2mol做还原剂,1mol做氧化剂,转移的电子为2mol,
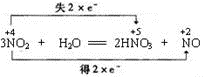
,
故答案为:

;
本题解析:
本题难度:一般
4、选择题 往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生.下列说法正确的是( )
A.该实验表明FeCl3有还原性
B.白色沉淀为BaSO3
C.该实验表明SO2有漂白性
D.反应后溶液酸性增强
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列说法正确的是( )
A.凡pH<7的雨水就可看作“酸雨”
B.燃烧不一定要有氧气参加,但燃烧一定是氧化还原反应
C.用NaClO溶液代替Cl2作为漂白剂是由于它难分解且在空气中可转化为HClO
D.“China”一词又指“青铜”,反映了在西方人眼中中国作为“青铜故乡”的形象
参考答案:BC
本题解析:
本题难度:简单