��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij��ҵ��Һ�ﺬ��FeCl2��CuCl2��FeCl3��Ϊ����ͭ���õ�������FeCl3��Һ���������ۺ����õ���Ҫ���̣�
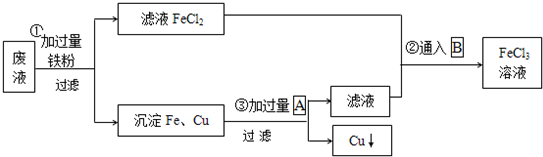
��1������������A��B�Ļ�ѧʽ��A______��B______��
��2���ڢٲ��Ļ�ѧ����ʽΪ______��______�ڢڲ�ͨ��B�Ļ�ѧ����ʽΪ______��
��3���ڢ۲��������A�����ӷ�Ӧ����ʽΪ��______��
�ο��𰸣���1������Cu��Fe���ɼ������ᣬ�õ�FeCl2��Cu����Ӧ�����ҺΪFeCl2������Cl2��Ӧ����FeCl3���ʴ�Ϊ��HCl��Cl2��
��2��CuCl2��FeCl3�м������ۣ��ֱ�����Fe+2FeCl3=3FeCl2��Fe+CuCl2=Cu+FeCl2���Ȼ�������������Ӧ��ת��Ϊ�Ȼ�������Ӧ�Ļ�ѧ����ʽΪ2FeCl2+Cl2 =2FeCl3��
�ʴ�Ϊ��Fe+2FeCl3=3FeCl2��Fe+CuCl2=Cu+FeCl2��2FeCl2+Cl2 =2FeCl3��
��3��Fe��Cu���ã��������ᷴӦ���ɶ������Cu����Ӧ�����ӷ���ʽΪFe+2H+=Fe2++H2�����ʴ�Ϊ��Fe+2H+=Fe2++H2����
���������
�����Ѷȣ�һ��
2������� ��12�֣�ÿ��2�֣� ����A��B��C��D��E��F���ֳ����������֪���ǣ������ӷֱ���K����Ag����Na����Ba2����Fe2����Al3���������ӷֱ���Cl����OH����AlO�� NO��SO��CO�������Ƿֱ����0.1 mol/L����Һ��������ʵ�飺
NO��SO��CO�������Ƿֱ����0.1 mol/L����Һ��������ʵ�飺
�ٲ����ҺA��C��E���ʼ��ԣ��Ҽ��ԣ�A>E>C��E����ɫ��dz��ɫ(����ɫ�ܲ����۲�)��
����B��Һ�еμ�ϡ��ˮ�������������ɳ����������ȫ���ܽ⣻
����F��Һ�еμ�ϡ���ᣬ��Һ����ػ�ɫ��������ɫ�������ɣ�
����D��Һ�е� ��Ba(NO3)2��Һ����
��Ba(NO3)2��Һ���� ������
������
(1)д��A��D��E��F�Ļ�ѧʽ��
A__________________��
D__________________��
E__________________��
F__________________��
(2)�����ӷ���ʽ����C��Һ�ļ��ԣ�________________________________________��
(3)д��ʵ����з�Ӧ�����ӷ���ʽ��_________________________________________��
�ο��𰸣�

�����������
�����Ѷȣ�һ��
3������� ��2.5g̼���ơ�̼�����ƺ��������ƵĹ���������ȫ�ܽ���ˮ���Ƴ�ϡ��Һ��Ȼ�������Һ����μ���1mol?L-1�����ᣬ�������������������CO2���������״������ϵ��ͼ��ʾ��
��1��д��OA����������Ӧ�����ӷ���ʽ______��______��
��2��������35mL����ʱ������CO2�����Ϊ______mL����״������
��3������ԭ�������NaOH��������̼���Ƶ���������______��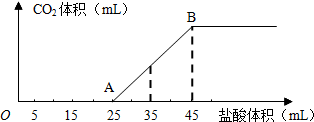
�ο��𰸣���1������Һ��̼���������������Ʒ�Ӧ����̼���ƣ����ͼ���֪����ʼû�ж�����̼�������ɣ����Ƴɵ�ϡ��Һ�е�����Ϊ̼���ƺ��������ƣ���OA��0��5mL�ȷ�������кͣ�
�����ӷ�Ӧ����ʽΪH++OH-�TH2O���ٷ���̼���������ᷴӦ����̼���������Ȼ��ƣ������ӷ�Ӧ����ʽΪCO32-+H+�THCO3-��
�ʴ�Ϊ��H++OH-�TH2O��CO32-+H+�THCO3-��
��2�����ͼ���֪��������35mL����ʱ��25��35mL����̼������������ķ�Ӧ���ɶ�����̼���壬
�����ɶ�����̼�����ʵ���Ϊn����������ʱ���ĵ�������ʵ���Ϊ��35-25����10-3L��1mol?L-1=0.01mol����
? HCO3-+H+�TCO2��+H2O
? 1? 1
?0.01mol ?n
11=0.01moln�����n=0.01mol����״���������Ϊ0.01mol��22.4L/mol=0.224L=224mL��
�ʴ�Ϊ��224��
��3����̼���ơ�̼�����ƺ��������Ƶ����ʵ����ֱ�Ϊx��y��z����
��x+y=1mol/L����0.045-0.025��L
��x+z=1mol/L��0.025L
��84g/mol?x+106g/mol?y+40g/mol?z=2.5g
�����٢ڢ�ʽ���x=0.01mol��y=0.01mol��z=0.015mol
��NaOH������Ϊ0.015mol��40g/mol=0.6g��
Na2CO3����������Ϊ0.01mol��106g/mol2.5g��100%=42.4%��
��ԭ�������NaOH������Ϊ0.6g��̼���Ƶ���������Ϊ42.4%��
���������
�����Ѷȣ�һ��
4��ѡ���� ���з�Ӧ����Ca2++ CO32��=CaCO3�� ��ʾ���ǣ�?��?
A������ʯ��ˮ��ͨ��CO2
B��Ca(NO3)2��Һ��Na2CO3��Һ���
C��CaCl2��Һ��BaCO3
D������ʯ��ˮ��Na2CO3��Һ���
�ο��𰸣�BD
�����������
�����Ѷȣ���
5��ѡ����
A��������������Һ��ͨ������CO2
OH����CO2===HCO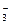
B���ð�ˮ��������SO2
2NH3��H2O��SO2===2NH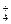 ��SO
��SO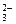 ��H2O
��H2O
C����������Һ�м��������ˮ
Al3����4NH3��H2O===AlO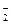 ��4NH
��4NH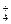 ��2H2O
��2H2O
D����Fe2(SO4)3��������Һ��ͨ������H2S