| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶԭ�Ӻ����������Ų����ʾ����Ƶ������ѵ��2017�����°棩(��)
��4��ij�������ͼ�Ԫ���γɵĻ�����侧���ṹ����ͼ��ʾ���þ���Ļ�ѧʽΪ______�� 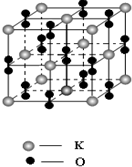 �ο��𰸣���1���ڶ�����Ԫ���γɵ�����������У�CO��CO2��NO��NO2��SO2��SO3�ȡ�����Ҫ����ǣ�O=C=O����2���Ҽ���2���м�������CO2?��ֱ���ͷ��ӣ���Cԭ�Ӳ�ȡsp?�ӻ�������OF2�ķ��ӹ�����H2O���ƣ�H2O�ķ��ӹ���ΪV�Σ�����OF2�ķ��ӹ���V�Σ�����ͬһ���ڣ������ң�Ԫ�صĵ縺�����������Ե��ĵ縺�ԣ����ĵ縺�ԣ�������ԭ�Ӱ뾶�ȵ�ԭ��С����S����������ǿ�������ĵ縺�Դ�? ��������� �����Ѷȣ�һ�� 3��ѡ���� ���и�ԭ�ӻ����ӵĵ����Ų�ʽ������� �ο��𰸣�B ��������� �����Ѷȣ��� 4��ѡ���� 2005���п�ѧ���ڡ�Science���Ϸ������ģ������������ij�ԭ�ӽṹAl13��?Al14�����������Ǽ��ȶ���Al13-��Al142+�ȣ�Al13��Al14�����ʺ����������ڱ���ijЩ����Ԫ�أ���֪�����೬ԭ�Ӿ���40���۵���ʱ���ȶ�������˵������ȷ���ǣ������� �ο��𰸣�A��������ԭ�ӡ�����������֮��Ϊ40��ʱ��������ȶ�״̬��Al13��39���۵��Ӽ���һ�����ӳ��ȶ���Al13-������������������ƣ���A��ȷ�� ��������� �����Ѷȣ��� 5������� (1)ԭ�ӹ�����ѵ��ӳ��ֵĸ���ԼΪ________�Ŀռ�Ȧ���������õ��ĵ���������ͼ�γ�Ϊԭ�ӹ���� �ο��𰸣�(1)90% ��������� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ�ر�֪ʶ�㡶������ԭ��.. | |
| �����Ŀ |