微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据表中短周期元素睦质的数据判断,
元素编号
元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧
原子半径/10-10m
0.66
1.36
1.23
1.10
0.99
1.54
0.70
1.18
|
最高或最低化合价
+2
+1
+5
+7
+1
+5
+3
-2
-3
-1
-3
|
下列说法正确的是( )
A.①⑧形成的化合物具有两性
B.⑦位于第2周期ⅥA族
C.④⑤形成的化合物是离子化合物
D.③的最高价氧化物对应的水化物碱性最强
参考答案:⑤有+7、-1价,则为Cl元素;④⑦都有+5、-3价,处于ⅤA族,④的原子半径较大,则④为P元素、⑤为N元素;③⑥都只有+1价,处于ⅠA族,⑥的原子半径较大,③的原子半径大于氯原子,故③为Li元素、⑥为Na元素;①有-2价,原子半径小于氯原子,故为O元素;②有+2价,原子半径大于Li原子,故为Mg元素;⑧有+3价,原子半径大于P原子,故为Al元素,
A.氧化铝是两性氧化物,故A正确;
B.N元素处于第二周期ⅤA族,故B错误;
C.三氯化磷、五氯化磷都属于共价化合物,故C错误;
D.③为Li元素,氢氧化锂的碱性比氢氧化钠弱,故D错误;
故选A.
本题解析:
本题难度:一般
2、填空题 以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。回答下列问题:
(1)镓为元素周期表第31号元素,镓原子价层电子排布图为__________________。
(2)氮所在主族中第一电离能最大的元素是___________(填元素符号,下同),镓所在主族中电负性最大的元素是_____________________。
(3)传统的氮化镓制备方法是采用CaCl3与NH3在一定条件下反应,该反应的化学方程式为_________________。
(4)氮化镓与金刚石具有相似的晶体结构,氮化镓中氮原子与镓原子之间以__________相结合,氮化镓属于______________晶体。
(5)下图是氮化镓的晶胞模型:
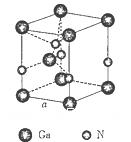
①氮化镓中镓原子的杂化方式为_______________,氮原子的配位数为__________________。
②氮化镓为立方晶胞,氮化镓的密度为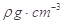 。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
参考答案:(1)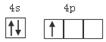
(2)N? B?
(3)GaCl3+NH3=GaN+3HCl
(4)共价键?原子
(5)①sp3 ?4?②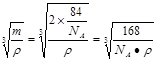
本题解析:(1)镓为元素周期表第31号元素,在元素周期表中的位置是位于第四周期第ⅢA。镓原子价层电子排布图为 。(2)氮在第ⅤA.在第ⅤA的元素中,由于N原子半径最小,原子核外的最外层电子处于半充满的稳定状态。所以其第一电离能最大。镓在元素周期表第ⅢA。该主族中元素中电负性最大的元素是原子半径最小的B元素。(3)用CaCl3与NH3在一定条件下反应制备氮化镓,根据质量守恒定律可得该反应的化学方程式为GaCl3+NH3=GaN+3HCl。?(4)氮化镓与金刚石具有相似的晶体结构,金刚石的C原子之间以共价键结合,是原子晶体。所以氮化镓中氮原子与镓原子之间以共价键相结合,氮化镓属于原子晶体。(5) ①每个镓与4个N形成共价键,这四个N构成正四面体结构。每个N与4个Ga形成共价键,这四个Ga构成正四面体结构。所以氮化镓中镓原子的杂化方式为sp3。氮原子的配位数为4. ②在每个晶胞中含有Ga:8×1/8+1=2,含有N:4× 1/4+1=2.即每个晶胞中含有2个GaN。氮化镓晶胞边长a。则
。(2)氮在第ⅤA.在第ⅤA的元素中,由于N原子半径最小,原子核外的最外层电子处于半充满的稳定状态。所以其第一电离能最大。镓在元素周期表第ⅢA。该主族中元素中电负性最大的元素是原子半径最小的B元素。(3)用CaCl3与NH3在一定条件下反应制备氮化镓,根据质量守恒定律可得该反应的化学方程式为GaCl3+NH3=GaN+3HCl。?(4)氮化镓与金刚石具有相似的晶体结构,金刚石的C原子之间以共价键结合,是原子晶体。所以氮化镓中氮原子与镓原子之间以共价键相结合,氮化镓属于原子晶体。(5) ①每个镓与4个N形成共价键,这四个N构成正四面体结构。每个N与4个Ga形成共价键,这四个Ga构成正四面体结构。所以氮化镓中镓原子的杂化方式为sp3。氮原子的配位数为4. ②在每个晶胞中含有Ga:8×1/8+1=2,含有N:4× 1/4+1=2.即每个晶胞中含有2个GaN。氮化镓晶胞边长a。则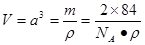 ,所以整理得:
,所以整理得: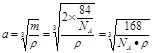 。
。
本题难度:困难
3、填空题 (15分)
已知:(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:

4FeCl3+2NH2OH・HCl 4FeCl2+N2O↑+6HCl+H2O
4FeCl2+N2O↑+6HCl+H2O
①Fe2+在基态时,价层电子排布式 。 ②羟胺(NH2OH)中N原子的杂化方式 ?。
③Fe2+与邻啡罗啉形成的配合物中,配位数为 。
(2)硫酸铜晶体的化学式也可以表达为Cu(H2O)4SO4・H2O晶体,该晶体中含有的化学键类型是
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、磷化镓及铜锢硒薄膜电池等。?其中元素P、As、Se第一电离能由小到大的顺序为: ?。
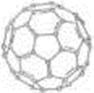

图1 ?图2
(4)① 有机太阳能固体电池材料含有高纯度C60,其结构如图1,则1 mol C60分子中π键的数目为 ,C60的晶胞结构如图2,则其配位数为_______若此晶胞的密度为ρg/cm3则两个最近C60间的距离为________cm(列式表达,已知阿伏伽德罗常数为NA)
② 如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周期电负性最小的原子可作为容体掺入C60晶体的空隙中,形成具有良好的超导性的掺杂C60化合物。若每个四面体空隙填入一个原子,则全部填满C60晶体的四面体空隙后,所形成的掺杂C60化合物的化学式为 。
参考答案:(1)①3d6;② sp3;③ 6;(2)离子键 共价键(配位键)
(3)Se< As< P?(4)① 30NA;12 ; ? ② K 2C60
? ② K 2C60
本题解析:(1)①Fe是26号元素,在Fe2+的核外有24个电子,在基态时,价层电子排布式3d6;②羟胺(NH2OH)中N原子的杂化方式sp3杂化; ③由化合物的结构简式可知:Fe2+与邻啡罗啉形成的配合物中,配位数为6;(2)在硫酸铜晶体Cu(H2O)4SO4・H2O中含有的化学键为离子键、共价键、配位键;(3)元素P、As是同一主族的元素,从上到下,原子半径增大,原子失去电子容易,所以第一电离能P>As;As、Se是同一周期的元素,原子半径As>Se,但是由于As原子的最外层的价电子处于该轨道的半充满的稳定状态,所以第一电离能As>Se.因此这三种元素的第一电离能由小到大的顺序为Se< As< P;(4)①在一个C60分子中含有60个C原子,每个C原子与连接的C原子形成了一个π键,而π键是两个原子所共有的,因此平均每个C原子含有的π键个数为1/2π键,。所以1 mol C60分子中π键的数目为60πNA÷2=30NA。由C60的晶胞结构示意图可知,它是立方面心结构,与每个C原子紧密连接的距离最近的C原子个数为(3÷8)÷2=12.即其配位数为12。每个晶胞中含有的C60分子个数是8×1/8+6×1/2=4;所以晶胞的边长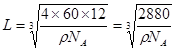 。根据晶胞示意图图可知两个最近C60间的距离为面对角线的一半,就是
。根据晶胞示意图图可知两个最近C60间的距离为面对角线的一半,就是 即为
即为 。②第四周期电负性最小的原子是K原子,由于每个顶点可形成1/4个四面体,一共有8个顶点,所以可形成2个正四面体。故可填充2个K原子,所形成的掺杂C60化合物的化学式为K 2C60。60化合物的化学式的确定的知识。
。②第四周期电负性最小的原子是K原子,由于每个顶点可形成1/4个四面体,一共有8个顶点,所以可形成2个正四面体。故可填充2个K原子,所形成的掺杂C60化合物的化学式为K 2C60。60化合物的化学式的确定的知识。
本题难度:一般
4、选择题 某化学课外活动小组甲同学欲制备收集A气体,乙同学欲制备收集B气体(制备方法、装置、试剂的化学式均相同).甲采用排水法收集到B气体,乙用排空气法却得到A气体.下列关于A、B两种气体的叙述不正确的是( )
A.A、B都是极性分子
B.A、B气体分子中均含有极性键
C.A为酸酐,B则不属于酸酐
D.A、B气体相对分子质量之差为16
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列说法正确的是(?)
A.H2O是一种非常稳定的化合物,这是由于氢键所致
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属晶体的熔点普遍都很高
参考答案:B
本题解析:氢键一般影响物质的物理性质,水分子稳定,是由于化学键的原因。干冰升华属于物理变化,破坏的是分子间作用力。金属晶体的熔点并不都是普遍很高,例如碱金属等。所以正确的答案是B。
本题难度:一般