微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某不纯的烧碱样品,含Na2CO3 3.8%(质量百分含量)、H2O 5.8%、NaHCO3 0.004%。取m g样品溶于40 m L 2 mol/L的盐酸后,并用2 mol/L Na OH溶液中和剩余的酸,在蒸发后可得干燥的固体的质量为(?)
A.4.68 g
B.5.58 g
C.2.34 g
D.3.34 g
参考答案:A
本题解析:完全反应后所得溶液的溶质为NaCl,根据Cl元素守恒,蒸发后所得NaCl的物质的量等于HCl的物质的量,所以m(NaCl)=0.04L×2mol/L×58.5g/mol=4.68g,故A项正确。
本题难度:一般
2、选择题 若某氖原子的质量是a g,12C的原子质量是b g,Na表示阿伏加德罗常数的值。下列说法错误的是(? )
A.该氖原子的摩尔质量为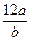 g
g
B.该氖原子的摩尔质量为aNa g・mol-1
C.w g该氖原子的物质的量为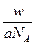 mol
mol
D.w g该氖原子所含的电子数是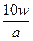
参考答案:A
本题解析:摩尔质量的单位为g・mol-1,A项错误;由摩尔质量的定义,摩尔质量与物质相对原子质量的关系及物质的量与物质质量、物质粒子数之间的关系可推知B、C、D项均正确。
本题难度:简单
3、选择题 现有等体积混合而成的4组气体:①NO2+NO、②NO2+O2、③HCl+N2、④Cl2+SO2. 现将其分别通入体积相同的试管中并立即倒立在足量水中,试管内水面上升的高度分别为h1、h2、h3、h4,则高度关系是 (? )
A.h4>h2>h3>h1
B.h4>h3>h2>h1
C.h2>h3>h1>h4
D.h3>h2>h1>h4
参考答案:A
本题解析:设试管的高度都是h,则根据3NO2+H2O=2HNO3+NO、4NO2+O2+2H2O=4HNO3、Cl2+SO2+2H2O=2HCl+H2SO4可知,①中水的高度是h/3、②中是5h/8、④水充满试管,氯化氢极易溶于水,而氮气不溶于水,所以水的高度是h/2,则答案选A。2等气体溶于水的有关计算
点评:该题的关键是根据物质的性质特别是化学性质,写出相关的化学方程式,逐一带入数据进行计算即可。
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值,下列说法中不正确的是
A.17g氨气中含有3NA对共用电子对
B.标准状况下4.48LN2与CO的混合物所含分子数为0.2NA
C.16g甲烷与足量的氯气在强光作用下最多可得4NA个HCl分子
D.0.2 mol C2H6O分子中一定存在0.2NA个碳碳单键
参考答案:D
本题解析:NH3中含有3对氮氢单键,17g氨气是1mol,故A正确;标准状况下4.48L气体是0.2mol,所以含有的分子数为0.2NA,而与气体的组成无关l,B正确;16g甲烷中含有4molH原子,因此最多可得4NA个HCl分子,C正确;分子式为C2H6O的化合物不一定是乙醇,也可能是甲醚,而甲醚分子内不存在碳碳单键,故D应是不正确的。
本题难度:简单
5、选择题 使5.6L CO2气体迅速通过Na2O2固体后得到4.48L气体(标准状况),这4.48L气体的质量为
A.6.4g
B.11g
C.8.2g
D.1.6g
参考答案:C
本题解析:过氧化钠和CO2反应的方程式为2NaO2+2CO2=2Na2CO3+O2,所以根据体积差可知,产生的氧气是5.6L-4.48L=1.12L,物质的量是0.05mol。则剩余CO2是3.36L,物质的量是0.15mol,所以气体的质量是0.05mol×32g/mol+0.15mol×44g/mol=8.2g,答案选C。
本题难度:简单