微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某500mL溶液中含0.1mol?Fe2+、0.2mol?Fe3+,加入0.2mol铁粉,待Fe3+完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变
A.0.4mol/L
B.0.6mol/L
C.0.8mol/L
D.1.0mol/L
参考答案:C
本题解析:由2Fe3++Fe===3Fe2+可知,铁粉过量,最终溶液中的Fe2+的物质的量为0.4mol,其浓度为0.8mol/L
本题难度:一般
2、选择题 某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中
A.至少存在5种离子
B.Cl-一定存在,且c(Cl?)≥0.4mol/L
C.SO42-、NH4+、一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在,K+可能存在
参考答案:B
本题解析:分析:加入过量NaOH溶液,加热,得到0.02mol气体,可知一定存在铵离子;
红褐色沉淀是氢氧化铁,1.6g固体为三氧化二铁,可知一定有Fe3+,一定没有CO32-;
4.66g不溶于盐酸的沉淀,硫酸钡沉淀,物质的量为:0.02mol;
根据以上数据推算存在离子,根据电荷守恒推算氯离子的存在及数据.
解答:由于加入过量NaOH溶液,加热,得到0.02mol气体,说明一定有NH4+,且物质的量为0.02mol;同时产生红褐色沉淀,说明一定有Fe3+,1.6g固体为氧化铁,物质的量为0.01mol,故有0.02molFe3+,一定没有CO32-;
? 4.66g不溶于盐酸的沉淀为硫酸钡,一定有SO42-,物质的量为0.02mol;
? 根据电荷守恒,一定有Cl-,至少 0.02mol×3+0.02-0.02mol×2=0.04mol,物质的量浓度至少 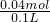 =0.4mol/L,
=0.4mol/L,
A、至少存在Cl-、SO42-、NH4+、Fe3+四种离子,故A错误;
B、根据电荷守恒,至少存在0.04molCl-,故B正确;
C、一定存在氯离子,故C错误;
D、Al3+无法判断是否存在,故D错误;
故选B.
点评:本题考查离子共存知识,做题是认真阅读、分析题中数据,合理分析,特别是氯离子的推断,难度中等.
本题难度:简单
3、选择题 下列过程与配合物的形成无关的是
A.向一定量的硝酸银溶液中加入氨水至过量
B.除去铁粉中的氧化铝可用强碱溶液
C.向一定量的硫酸铜溶液中加入氨水至沉淀消失
D.向Fe3+溶液中加入KSCN溶液后溶液呈血红色
参考答案:B
本题解析:
本题难度:困难
4、选择题 下列反应中氯元素被氧化的是
A.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
B.5Cl2+I2+6H2O=10HCl+2HIO3
C.2NaCl+2H2O2NaOH+Cl2↑+H2↑
D.MnO2+4HCl=MnCl2+2H2O+Cl2
参考答案:CD
本题解析:分析:反应中氯元素被氧化,说明氯元素在反应中失电子化合价升高被氧化,据此分析解答.
解答:A.该反应中,氯元素既有化合价升高的也有化合价降低的,所以氯元素既被氧化又被还原,故A不符合;
B.该反应中,氯元素得电子化合价降低,碘元素失电子化合价升高,所以氯元素被还原,故B不符合;
C.该反应中,氯元素失电子化合价升高,氢元素得电子化合价降低,所以氯元素被氧化,故C符合;
D.该反应中,氯元素失电子化合价升高,锰元素得电子化合价降低,所以氯元素被氧化,故D符合;
故选CD.
点评:本题考查氧化还原反应,明确元素化合价是解本题关键,难度不大.
本题难度:困难
5、选择题 下列物质中,不可作漂白剂的是
A.SO2
B.Ca(C1O)2
C.Na2SiO3
D.NaClO
参考答案:C
本题解析:分析:能作漂白剂的物质常见的有三类:1、具有强氧化性的物质(如HClO、NaCl0、Ca(C1O)2);2、能与有色物质化合生成不稳定无色物质(如SO2);3、具有吸附性的物质(如活性炭).
解答:A.SO2能与有色物质化合生成不稳定无色物质,可作漂白剂,故A不选;
B.Ca(C1O)2具有强氧化性,能使有色物质褪色,可作漂白剂,故B不选;
C.Na2SiO3不具有漂白性,不能使有色物质褪色,则不可作漂白剂,故C选;
D.NaClO具有强氧化性,能使有色物质褪色,可作漂白剂,故D不选;
故选C.
点评:本题考查漂白剂,熟悉常见的漂白剂及漂白原理是解答本题的关键,题目难度不大,注意硅酸钠的水溶液具有粘合性,而不具有漂白性.
本题难度:一般