微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 同温同压下,等体积的两种气体14N16O和13C16O,下列判断正确的是?
A.中子数相同
B.分子数不同
C.质子数相同
D.气体质量相同
参考答案:A
本题解析:A正确,14N16O的中子数为7+8=15,13C16O的中子数为7+8=15。
B错误,根据阿伏加德罗定律,同温同压,气体体积相同,气体分子物质的量相同。
C错误,14N16O质子数为7+8=15,13C16O质子数为6+8=14。
D错误,两种物质的摩尔质量不相同,在物质的量相等的情况下,质量不相同。
本题难度:一般
2、填空题 过氧乙酸是一种弱酸性氧化剂,广泛用作漂白剂和高效杀菌消毒剂等。
Ⅰ、制备:冰醋酸与H2O2浓溶液按体积比1:1混合,加入适量浓硫酸,控制温度5℃~30℃,搅拌30min并静置4~6h。
反应原理为:H2O2+CH3COOH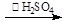
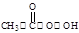 (过氧乙酸)+H2O
(过氧乙酸)+H2O
Ⅱ、含量测定:称取5.0000g过氧乙酸试样(液体),稀释至100mL备用。取上述稀释后过氧乙酸试样5.00mL,用0.0100 mol・L-1KMnO4溶液滴定到终点以除去其中的H2O2,随即加入10%KI溶液10mL,加入0.5%淀粉溶液3滴,摇匀,并用0.0500 mol・L-1Na2S2O3标准溶液滴定到蓝色刚好褪去(离子反应方程式为:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3标准溶液的总体积为20.00mL。
(1)制备过氧乙酸时,温度不宜过高,其原因可能是?。
(2)稀释样品时,除用到容量瓶及烧杯外,还用到的玻璃仪器有?、?。
(3)过氧乙酸溶液与KI反应的离子方程式为?。
(4)通过计算确定原试样中过氧乙酸的质量分数(写出计算过程)。?。
参考答案:
(1)温度过高,过氧化氢会发生分解;
(2)玻璃棒、胶头滴管。
(3)CH3COOOH+2H++2I-=I2+CH3COOH+H2O?
(4)
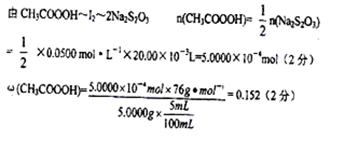
本题解析:(1)温度过高时过氧化氢会分解不能保证其和醋酸充分反应;(2)稀释样品时,还要用到胶头油管取液体,用玻璃棒在溶解时要搅拌。
(3)根据氧化还原反应原理,碘离子被氧化为碘单质,过氧乙酸溶液被还原为乙酸分子,故反应方程式如答案所示。
(4)根据两个化学方程式找出关系式如下:
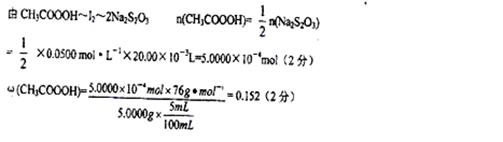
本题难度:一般
3、计算题 (8分)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
①取25mL甲溶液,向其中缓慢滴入乙溶液15mL,共收集到112mL(标准状况)气体。
②取15mL乙溶液,向其中缓慢滴入甲溶液25mL,共收集到56mL(标准状况)气体。
(1)判断:甲是?溶液,乙是?溶液;(均填化学式)
(2)甲溶液的物质的量浓度为?mol/L,乙溶液的物质的量浓度
为?mol/L,?(要求写出计算过程)。
参考答案:(1)HCl(1分) Na2CO3(1分)
(2) 0.4(3分)? 0.5(3分)
本题解析:略
本题难度:一般
4、选择题 10g?10%的氢氧化钠溶液稀释成50mL,所得氢氧化钠溶液的物质的量浓度为( )
A.0.02mol/L
B.0.05mol/L
C.0.25mol/L
D.0.5mol/L
参考答案:10g10%的氢氧化钠溶液中溶质的质量为10g×10%=1g,
则NaOH的物质的量为1g40g/mol=0.025mol,
所以氢氧化钠溶液的物质的量浓度为0.025mol0.05L=0.5mol/L,
故选D.
本题解析:
本题难度:一般
5、选择题 下列物质中所含分子物质的量最多的是
A.56gN2
B.1.5molO2
C.标准状态下22.4LCl2
D.3.01×1023个硫酸分子