A����������
�ο��𰸣�C
������������ݷ���ʽ��֪����Ӧ���������ġ����ȵĿ��淴Ӧ�����������¶�ƽ�����淴Ӧ�����ƶ�������������ƽ����Է����������䣬A����ȷ���ı�ѹǿ��ƽ�ⲻ�ƶ���A�ĺ������䣬B����ȷ������A��Ũ�ȣ�ƽ��������Ӧ�����ƶ���B��ת��������C��ȷ���������ܸı�ƽ��״̬������A�ĺ����Dz���ģ�D����ȷ����ѡC��
�����Ѷȣ�һ��
2��ѡ���� ���ڻ�ѧ��Ӧ3W(g)��2X(g)===4Y(g)��3Z(g)�����з�Ӧ���ʹ�ϵ�У���ȷ����
[? ]
A��v(W)��3v(Z)����������
B��2v(X)��3v(Z)
C��2v(X)��v(Y)? ?
D��3v(W)��2v(X)
�ο��𰸣�C
���������
�����Ѷȣ���
3������� ��ÿ�ո�3�֣���18�֣���ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ���˺���������д��������õĴ������������֡�
����1����ԭ������
�÷��Ĺ�������Ϊ
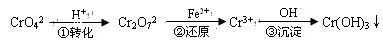
���еڢٲ�����ƽ�⣺2CrO42������ɫ��+2H+ Cr2O72������ɫ��+H2O Cr2O72������ɫ��+H2O
��1����ƽ����ϵ��pH=2������Һ��?ɫ.
��2���ڢڲ��У���ԭ1mol Cr2O72�����ӣ���Ҫ________mol��FeSO4��7H2O��
��3���ڢ۲����ɵ�Cr(OH)3����Һ�д������³����ܽ�ƽ�⣺
Cr(OH)3(s) Cr3+(aq)+3OH��(aq) Cr3+(aq)+3OH��(aq)
�����£�Cr(OH)3���ܶȻ�Ksp��c(Cr3+)��c3(OH��)��10-32��Ҫʹc(Cr3+)����10-5mol/L����Һ��pHӦ����?��
����2����ⷨ
�÷���Fe���缫��⺬Cr2O72�������Է�ˮ�����ŵ����У�������������ҺpH���ߣ�����Cr(OH)3������
��4����Fe���缫��������ӦʽΪ��
?��
��5��������������ҺpH���ߵ�ԭ���ǣ��õ缫��Ӧ���ͣ�?����Һ��ͬʱ���ɵij�������?��
�ο��𰸣���ÿ��3�ּ�18�֣���1����?��2��6?��3��5
��4�� Fe��2e����Fe2+
��5��2H++2e����H2��?Fe(OH)3
���������
��������1���������������ƽ���Ӱ��������ƽ���ƶ����Ӷ�ȷ������Ũ�ȴ�С������ȷ����ɫ�仯��
��2���ж�ƽ��״̬�ķ�����V��=V�棬�����ֵ�Ũ�ȱ��ֲ��䣬���ܱ�������ֲ�����˵���Ѵ�ƽ�⣻
��3�����ݵ�ʧ�����غ������㣻
��4�������ܶȻ��������м��㣻
��5�������ǻ��Ե缫ʱ����������ʧ���ӣ����������ӣ�
��6����ҺPH���ߵ�ԭ������Һ��������Ũ�ȼ��٣����������������õ��ӣ�PH���ߣ�����������Ũ����������Ũ���ݵij˻������ܶȻ������Խ��������ӻ������������������
����⣺��1��c��H+������ƽ��2CrO42-����ɫ��+2H+ Cr2O72-����ɫ��+H2O���ƣ���Һ�ʳ�ɫ�� Cr2O72-����ɫ��+H2O���ƣ���Һ�ʳ�ɫ��
��2��ƽ��ʱ�����ʵ�Ũ�Ȳ��ٸı䣬����Һ����ɫ���ٸı䣻
��3�����ݵ��ӵ�ʧ�غ��֪����ԭ1molCr2O72-���ӵõ�Cr3+���õ��ӣ�2����6-3���T6mol����ҪFeSO4?7H2O�����ʵ���Ϊ��6�£�3-2���T6��
��4����c��Cr3+��=10-5mol/Lʱ����Һ��c��OH-��=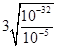 =10-9mol/L��c��H+���T =10-9mol/L��c��H+���T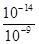
��pH=5����Ҫʹc��Cr3+������10-5mol/L����Һ��pHӦ����5��
��5���ڵ�ⷨ�����У�����������������ӦΪFe-2e-�TFe2+�����ṩ��ԭ��Fe2+��
��6��������������ҺpH���ߵ�ԭ����ˮ���������H+�ŵ�����H2��ͬʱ������������OH-��������Һ�е�Fe3+Ҳ��ת��ΪFe��OH��3������
�ʴ�Ϊ����1���ȣ���2��c����3��6����4��5����5��������ӦΪFe-2e-�TFe2+���ṩ��ԭ��Fe2+����6��2H++2e-�TH2����Fe��OH��3��
�����������ۺϿ����˻�ѧƽ��ԭ����������ԭ��Ӧ�������ܽ�ƽ��͵绯ѧ֪ʶ�����ݣ�����ʱҪ���������Ϣ��������ԭ�����н��
�����Ѷȣ���
4��ѡ���� ij��ѧ����С���о���������������ʱ���ı�ijһ�����Ի�ѧƽ���Ӱ�죬�õ����±仯���ɣ�ͼ��p��ʾѹǿ��t��ʾ�¶ȣ�n��ʾ���ʵ�������
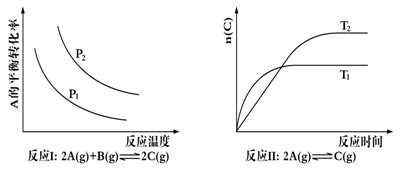
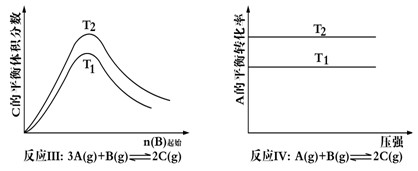
�������Ϲ����жϣ����н�����ȷ����
A����Ӧ���H> 0��P2>P1
B����Ӧ���H<0��T1>T2
C����Ӧ���H> 0,T2>T1;���H<0,T2<T1
D����Ӧ����H<0��T2>T1
�ο��𰸣�BC
�����������ӦI���¶�Խ�ߣ�ת����Խ�ͣ�˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ���������Ӧ�Ƿ��ȷ�Ӧ��A����ȷ����Ӧ���У�T1��ʾ�������Ե���ƽ��״̬�������¶���T1>T2�����¶�Խ�ߣ�C�ĺ���Խ�ͣ�˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ���������Ӧ�Ƿ��ȷ�Ӧ��B��ȷ����Ӧ���У��������Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�ƽ�����淴Ӧ�����ƶ���������ĺ������ͣ���T2<T1��ͬ���������������Ӧ�����ȷ�Ӧ���������¶ȣ�ƽ��������Ӧ�����ƶ���������ĺ�������T2��T1��C��ȷ����Ӧ�������жϷ�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ������ȷ����ѡBC��
�����Ѷȣ�һ��
5�������� ���������ڼ����������ܹ��ֽ��һ���������������÷�Ӧ���е�45 sʱ���ﵽƽ��(NO2Ũ��ԼΪ
0.0125 mol/L)����ͼ�е����߱�ʾ���������ֽ���ǰ25s�ڵķ�Ӧ���̡�
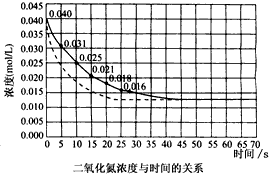
��1�������ǰ20s��������ƽ���������ʡ�
��2������Ӧ������70 s������ͼ����ʵ����25s��70s�ķ�Ӧ�������ߡ�
��3�����ڷ�Ӧ��ʼʱ�������(��������������)������ͼ�������������������ķ�Ӧ�������ߡ�
��4��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ__________��
�ο��𰸣���1��5.5��10-4mol/(L��s)
��2����ͼ��ʵ��
��3����ͼ�����ߡ� ��4��K��c(NO)c(O2)/[c(NO2)]2 ��4��K��c(NO)c(O2)/[c(NO2)]2
���������
�����Ѷȣ�һ��
|